Bahan aktif: Docetaxel
TAXOTERE 20 mg / 0.5 ml pekat dan pelarut untuk larutan untuk infusi
Sisipan pakej Taxotere tersedia untuk pek:- TAXOTERE 20 mg / 0.5 ml pekat dan pelarut untuk larutan untuk infusi
- TAXOTERE 80 mg / 2 ml pekat dan pelarut untuk larutan untuk infusi
- TAXOTERE 20 mg / 1 ml pekat untuk larutan untuk infusi
- TAXOTERE 80 mg / 4 ml pekat untuk penyelesaian untuk infusi
- TAXOTERE 160 mg / 8 ml pekat untuk penyelesaian untuk infusi
Mengapa Taxotere digunakan? Untuk apa itu?
Nama ubat ini adalah TAXOTERE. Nama bahan aktifnya adalah docetaxel.
Docetaxel adalah bahan yang berasal dari daun jarum seperti daun tanaman yew dan tergolong dalam kumpulan anti-barah yang disebut taksana.
TAXOTERE telah diresepkan oleh doktor anda untuk merawat barah payudara, bentuk barah paru-paru tertentu (barah paru-paru sel kecil), barah prostat, barah gastrik, atau barah kepala dan leher:
- Untuk rawatan barah payudara lanjut, TAXOTERE boleh diberikan sendiri atau bersama dengan doxorubicin, atau trastuzumab, atau capecitabine.
- Untuk rawatan barah payudara awal dengan atau tanpa penglibatan kelenjar getah bening, TAXOTERE boleh diberikan bersama dengan doxorubicin dan siklofosfamid.
- Untuk rawatan barah paru-paru, TAXOTERE boleh diberikan sendiri atau bersama dengan cisplatin.
- untuk rawatan barah prostat, TAXOTERE diberikan dalam kombinasi dengan prednisone atau prednisolone.
- untuk rawatan barah gastrik metastatik, TAXOTERE diberikan bersama dengan cisplatin dan 5-fluorouracil.
- untuk rawatan barah kepala dan leher, TAXOTERE diberikan bersama dengan cisplatin dan 5-fluorouracil.
Kontraindikasi Apabila Taxotere tidak boleh digunakan
Anda tidak boleh mengambil TAXOTERE
- jika anda alah (sensitif) terhadap docetaxel atau bahan-bahan lain dari Taxotere;
- jika jumlah sel darah putih anda terlalu rendah;
- jika anda mempunyai masalah hati yang teruk;
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Taxotere
Sebelum setiap rawatan dengan TAXOTERE perlu dilakukan ujian darah yang diperlukan untuk menentukan sama ada terdapat sel darah yang cukup dan apakah hati cukup aktif. Sekiranya terdapat perubahan pada sel darah putih, demam atau jangkitan juga mungkin berlaku.
Beritahu doktor, ahli farmasi hospital atau jururawat anda jika anda mempunyai masalah penglihatan. Sekiranya anda mempunyai masalah penglihatan, terutamanya penglihatan kabur, anda harus segera memeriksa mata dan penglihatan anda.
Sekiranya anda mengalami masalah paru-paru akut atau jika gejala anda yang ada semakin teruk (demam, sesak nafas atau batuk), beritahu doktor, ahli farmasi hospital atau jururawat anda dengan segera. Doktor anda mungkin segera menghentikan rawatan.
Anda akan diminta untuk melakukan rawatan pencegahan dengan kortikosteroid oral seperti dexamethasone sehari sebelum pemberian TAXOTERE dan meneruskannya selama satu atau dua hari selepas itu untuk mengurangkan beberapa kesan sampingan yang mungkin timbul berikutan infus TAXOTERE, khususnya alergi reaksi dan pengekalan cecair (bengkak tangan, kaki, kaki, atau kenaikan berat badan).
Semasa rawatan, anda mungkin memerlukan ubat untuk mengekalkan jumlah sel darah anda.
Interaksi Dadah atau makanan mana yang boleh mengubah kesan Taxotere
Beritahu doktor atau ahli farmasi hospital anda jika anda mengambil atau baru-baru ini mengambil ubat lain, termasuk ubat yang diperoleh tanpa preskripsi. Ini kerana TAXOTERE atau ubat lain mungkin tidak berfungsi seperti yang diharapkan dan anda mungkin lebih terdedah kepada kesan sampingan.
Amaran Penting untuk mengetahui bahawa:
Kehamilan, penyusuan dan kesuburan
Minta nasihat doktor anda sebelum mengambil sebarang ubat.
TAXOTERE TIDAK boleh diberikan sekiranya anda hamil kecuali dinyatakan dengan jelas oleh doktor anda.
Anda tidak boleh hamil semasa dirawat dengan ubat ini dan mesti menggunakan langkah-langkah kontraseptif yang mencukupi semasa terapi kerana TAXOTERE mungkin berbahaya bagi bayi. Sekiranya anda hamil semasa rawatan, sila beritahu doktor anda dengan segera. Anda tidak boleh menyusu semasa mengambil TAXOTERE.
Sekiranya anda seorang lelaki yang dirawat dengan TAXOTERE, disarankan untuk tidak membiak selama dan hingga 6 bulan setelah rawatan dan bertanya tentang penyimpanan sperma sebelum rawatan kerana docetaxel boleh mengganggu kesuburan lelaki.
Memandu dan menggunakan mesin:
Tidak ada kajian mengenai kesan keupayaan memandu dan menggunakan mesin yang dilakukan.
Dos dan kaedah penggunaan Cara menggunakan Taxotere: Dos
TAXOTERE akan diberikan kepada anda oleh profesional penjagaan kesihatan.
Dos biasa:
Dos bergantung kepada berat badan dan keadaan kesihatan umum anda. Doktor anda akan mengira luas permukaan badan anda dalam meter persegi (m2) dan menentukan dos yang perlu anda terima.
Kaedah dan kaedah pentadbiran:
TAXOTERE akan diberikan kepada anda melalui infus intravena (penggunaan intravena). Infusi akan berlangsung sekitar 1 jam dan akan berlangsung di hospital.
Kekerapan pentadbiran:
Infusi biasanya akan diberikan kepada anda 3 minggu sekali.
Doktor anda mungkin mengubah dos dan kekerapan pentadbiran berkaitan dengan ujian darah anda, keadaan umum anda dan tindak balas anda terhadap TAXOTERE. Khususnya, beritahu doktor anda jika anda mengalami cirit-birit, sakit mulut, mati rasa, kesemutan, demam, dan tunjukkan hasil ujian darah anda. Maklumat ini akan membolehkannya memutuskan sama ada pengurangan dos diperlukan. Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini, berjumpa dengan doktor atau ahli farmasi hospital anda.
Kesan Sampingan Apakah kesan sampingan dari Taxotere
Seperti semua ubat, ubat ini boleh menyebabkan kesan sampingan, walaupun tidak semua orang mendapatnya.
Doktor anda akan membincangkannya dengan anda dan menerangkan potensi risiko dan faedah rawatan.
Reaksi buruk TAXOTERE yang paling kerap dilaporkan adalah: penurunan bilangan sel darah merah atau putih, keguguran rambut, mual, muntah, radang di mulut, cirit-birit dan keletihan
Sekiranya TAXOTERE diberikan kepada anda bersama dengan agen kemoterapi lain, tahap kesan sampingan mungkin meningkat.
Reaksi alahan berikut mungkin berlaku semasa infusi di hospital (boleh mempengaruhi lebih dari 1 dari 10 orang):
- memerah, reaksi kulit, gatal-gatal
- sesak dada, kesukaran bernafas
- demam atau menggigil
- sakit belakang
- tekanan rendah
Reaksi yang lebih teruk mungkin berlaku.
Keadaan anda akan dipantau dengan teliti oleh kakitangan hospital semasa rawatan. Beritahu kakitangan hospital dengan segera sekiranya anda mengetahui kesannya.
Kesan sampingan yang disenaraikan di bawah mungkin berlaku pada waktu antara dua infus TAXOTERE, dan kekerapannya mungkin berbeza-beza bergantung pada ubat kombinasi yang anda ambil:
Sangat biasa (boleh mempengaruhi lebih daripada 1 dari 10 orang):
- jangkitan, penurunan bilangan sel darah merah (anemia) atau sel darah putih (yang terakhir penting dalam memerangi jangkitan) dan platelet
- demam: dalam kes ini anda mesti segera memberitahu doktor
- reaksi alahan seperti yang dinyatakan di atas
- kehilangan selera makan (anoreksia)
- insomnia
- rasa kebas atau kesemutan atau sakit pada sendi atau otot
- sakit kepala
- perubahan rasa
- keradangan mata atau peningkatan mata yang koyak
- bengkak disebabkan oleh saliran limfa yang tidak mencukupi
- kesukaran bernafas
- kehilangan lendir dari hidung; keradangan tekak dan hidung; batuk
- mimisan
- keradangan di mulut
- sakit perut termasuk loya, muntah dan cirit-birit, sembelit
- sakit perut
- senak
- keguguran rambut (pertumbuhan rambut kembali normal dalam kebanyakan kes)
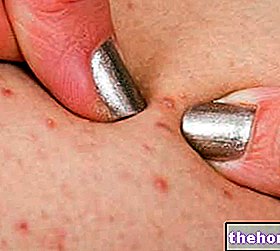
- kemerahan dan pembengkakan telapak tangan atau tapak kaki, yang boleh menyebabkan pengelupasan kulit (ini juga boleh berlaku pada lengan, muka atau badan)
- perubahan warna kuku, yang boleh mengelupas
- sakit otot; sakit belakang atau sakit tulang
- perubahan atau ketiadaan haid
- bengkak tangan, kaki, kaki
- keletihan atau gejala selesema
- kenaikan atau penurunan berat badan
Biasa (boleh mempengaruhi sehingga 1 dari 10 orang):
- kandidiasis oral
- penyahhidratan
- pening
- gangguan pendengaran
- penurunan tekanan darah; degupan jantung yang tidak teratur atau cepat
- kegagalan jantung
- esofagitis
- mulut kering
- kesukaran atau kesakitan ketika menelan
- pendarahan
- peningkatan enzim hati (oleh itu keperluan untuk ujian darah biasa)
Tidak biasa (boleh mempengaruhi sehingga 1 dari 100 orang):
- pengsan
- di tempat suntikan reaksi kulit, phlebitis (radang urat) atau bengkak
- keradangan usus besar, usus kecil; perforasi usus.
- pembentukan gumpalan darah
Kekerapan tidak diketahui:
- penyakit paru-paru interstitial (radang paru-paru yang boleh menyebabkan batuk dan kesukaran bernafas. Keradangan paru-paru juga dapat berkembang apabila rawatan docetaxel diberikan bersamaan dengan radioterapi)
- radang paru-paru (jangkitan paru-paru)
- fibrosis paru (parut dan penebalan pada paru-paru menyebabkan sesak nafas)
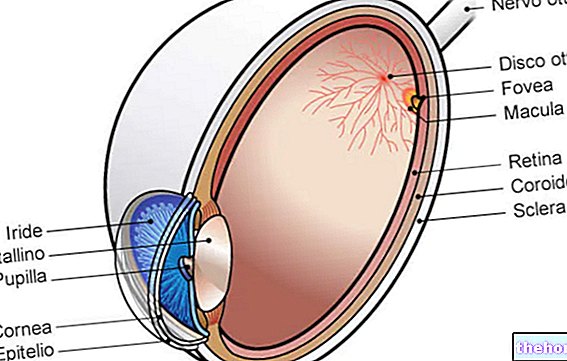
- penglihatan kabur kerana pembengkakan retina di dalam mata (edema makular cystoid)
- penurunan natrium dalam darah.
Melaporkan kesan sampingan
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor, ahli farmasi hospital atau jururawat anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional yang disenaraikan dalam Lampiran V *. Dengan melaporkan kesan sampingan, anda dapat membantu memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
Jauhkan ubat ini dari pandangan dan jangkauan kanak-kanak.
Jangan gunakan ubat ini selepas tarikh luput yang tertera pada kadbod, lepuh dan botol.
Jangan simpan di atas 25 ° C atau di bawah 2 ° C.
Simpan ubat dalam bungkusan asli untuk melindunginya dari cahaya langsung
Larutan yang telah dicairkan mesti digunakan sejurus selepas penyediaan, walaupun kestabilan kimia-fizikal larutan tersebut telah ditunjukkan selama 8 jam jika disimpan antara + 2 ° C hingga + 8 ° C atau pada suhu bilik (di bawah 25 C) .
Penyelesaiannya harus digunakan dalam 4 jam jika disimpan pada suhu bilik (di bawah 25 ° C).
Apa yang terkandung dalam botol pekat TAXOTERE:
Bahan aktifnya adalah docetaxel (sebagai trihydrate). Setiap ml larutan docetaxel mengandungi 40 mg docetaxel (anhidrat). Satu botol mengandungi 20 mg / 0.5 ml docetaxel. Bahan-bahan lain adalah polisorbat 80 dan asid sitrik.
Apa yang terdapat dalam botol pelarut:
13% (b / b) 95% etanol dalam air untuk suntikan.
Penerangan tentang bagaimana TAXOTERE dan kandungan peknya:
TAXOTERE 20 mg / 0.5 ml pekat untuk larutan infus adalah larutan jernih, likat, kuning hingga kuning-coklat.
Setiap pek mengandungi
- botol dos pekat tunggal dan,
- botol pelarut dos tunggal
Maklumat berikut ditujukan untuk profesional kesihatan sahaja.
PANDUAN PERSEDIAAN UNTUK TAXOTERE 20 mg / 0.5 ml CONCENTRATE FOR SOLUTION FOR INFUSION DAN SOLVENT BERKAITAN UNTUK TAXOTERE
Penting untuk anda membaca keseluruhan kandungan panduan ini sebelum menyediakan penyelesaian larutan TAXOTERE dan penyelesaian TAXOTERE untuk infus.
1. FORMULASI
TAXOTERE 20 mg / 0,5 ml pekat untuk larutan untuk infus adalah larutan berwarna kuning hingga kuning-coklat jernih yang mengandungi 40 mg / ml docetaxel (anhidrat) dalam polysorbate 80 dan asid sitrik. Pelarut TAXOTERE adalah larutan 13% (b / b) 95% etanol dalam air untuk suntikan.
2. PEMBENTANGAN
TAXOTERE dibekalkan dalam botol dos tunggal.
Setiap pek mengandungi satu botol TAXOTERE (20 mg / 0,5 ml) dan satu botol pelarut yang sesuai untuk TAXOTERE dalam pek lepuh.
Botol TAXOTERE mesti disimpan antara + 2 ° C hingga + 25 ° C dilindungi dari cahaya.
TAXOTERE tidak boleh digunakan selepas tarikh luput yang tertera pada kadbod, lepuh dan botol.
2.1 Botol TAXOTERE 20 mg / 0.5 ml:
- Botol TAXOTERE 20 mg / 0,5 ml, berkapasitas 7 ml, terbuat dari kaca jernih dengan penutup hijau yang dapat ditanggalkan.
- Botol TAXOTERE 20 mg / 0.5 ml mengandungi larutan docetaxel dalam polysorbate 80 pada kepekatan 40 mg / ml.
- Setiap botol TAXOTERE 20 mg / 0.5 ml mengandungi 0.5 ml larutan docetaxel 40 mg / ml dalam polysorbate 80 (isian isian: 24.4 mg / 0.61 ml). Overdosis ini berlaku semasa pengembangan TAXOTERE untuk mengimbangi kehilangan cecair semasa penyediaan larutan yang telah diencerkan (lihat bahagian 4) kerana berbuih, lekatan pada dinding botol dan 'ruang mati'. Overdosis ini memastikan bahawa selepas pencairan dengan keseluruhan kandungan botol pelarut yang disertakan dengan TAXOTERE, jumlah minimum larutan yang boleh diekstraksi adalah 2 ml, mengandung 10 mg / ml docetaxel, yang sesuai dengan kandungan yang dinyatakan pada label 20 mg / 0, 5 ml setiap botol.
2.2 Pelarut untuk botol TAXOTERE 20 mg / 0.5 ml:
- Pelarut untuk TAXOTERE 20 mg / 0.5 ml terkandung dalam botol kaca jernih 7 ml dengan penutup flip-off yang jelas.
- Pelarut untuk TAXOTERE 20 mg / 0.5 ml terdiri daripada larutan 13% (b / b) 95% etanol dalam air untuk suntikan.
- Setiap botol pelarut untuk TAXOTERE 20 mg / 0.5 ml mengandungi 1.98 ml larutan. Isipadu ini dikira berdasarkan isipadu sebenar botol TAXOTERE 20 mg / 0.5 ml. Menambah keseluruhan kandungan botol pelarut ke dalam TAXOTERE 20 mg / 0,5 ml memastikan bahawa larutan 10 mg / ml docetaxel diperolehi.
3. SARANAN UNTUK PENGENDALIAN SELAMAT
TAXOTERE adalah ubat antineoplastik dan, seperti produk berpotensi toksik lain, perlu berhati-hati dalam menangani dan menyediakan penyelesaian. Penggunaan sarung tangan adalah disyorkan.
Sekiranya TAXOTERE dalam bentuk pekat, larutan pra-dicairkan atau larutan infus harus bersentuhan dengan kulit, basuh segera dan bersih dengan sabun dan air. Sekiranya TAXOTERE dalam bentuk pekat, pra-dicairkan atau dalam larutan untuk infusi harus bersentuhan dengan membran mukus, basuh segera dan bersih dengan air.
4. PERSEDIAAN UNTUK PENTADBIRAN INTRAVENOUS
4.1 Penyediaan larutan taksil TAXOTERE (10 mg docetaxel / ml)
4.1.1 Sekiranya botol disimpan di dalam peti sejuk, biarkan jumlah kotak TAXOTERE yang diperlukan pada suhu bilik (di bawah 25 ° C) selama 5 minit.
4.1.2 Dengan menggunakan jarum suntik bertahap dengan jarum, tarik secara keseluruhan secara aseptikal seluruh isi botol pelarut untuk TAXOTERE dengan membalikkan sebahagian botol.
4.1.3 Suntikan keseluruhan kandungan jarum suntik ke dalam botol TAXOTERE yang sesuai
4.1.4 Tanggalkan jarum suntik dan jarum dan campurkan larutan secara manual dengan membalikkan berulang kali selama 45 saat.Jangan goncang.
4.1.5 Biarkan botol larutan yang telah dilarutkan selama 5 minit pada suhu bilik (di bawah 25 ° C) dan kemudian periksa bahawa larutan itu jelas dan homogen (berbuih normal walaupun selepas 5 minit kerana kandungan polysorbate 80 dalam perkataan) .
Larutan yang telah diencerkan mengandungi 10 mg / ml docetaxel dan mesti digunakan sejurus selepas penyediaan, walaupun kestabilan kimia-fizikal larutan ini telah ditunjukkan selama 8 jam jika disimpan antara + 2 ° C dan + 8 C atau ambien suhu (di bawah 25 C).
4.2 Penyediaan penyelesaian untuk infusi
4.2.1 Sebilangan besar larutan larutan mungkin diperlukan untuk mendapatkan dos pesakit yang diperlukan. Berdasarkan dos pesakit yang diperlukan dalam mg, tarik isipadu larutan larutan yang sesuai yang mengandungi 10 mg / ml docetaxel dari sebilangan botol yang sesuai menggunakan jarum suntikan bertahap. Sebagai contoh, untuk dos docetaxel 140 mg, 14 ml larutan docetaxel yang telah diprutilasi harus ditarik.
4.2.2 Suntikan isipadu larutan yang diencerkan ke dalam beg atau botol 250 ml yang mengandungi larutan glukosa 5% atau larutan natrium klorida 9 mg / ml (0,9%) untuk infus. Sekiranya dos docetaxel lebih besar daripada 200 mg diperlukan, gunakan jumlah larutan yang lebih besar untuk infus sehingga kepekatan docetaxel tidak melebihi 0,74 mg / ml.
4.2.3 Campurkan beg atau botol secara manual dengan gerakan memutar.
4.2.4 Penyelesaian TAXOTERE untuk infus harus digunakan dalam 4 jam dan harus diberikan sebagai infus 1 jam, secara aseptik, pada suhu bilik (di bawah 25 C) dan dalam keadaan cahaya normal. Dokumen disediakan oleh AIFA pada 05/27/2015 243
4.2.5 Seperti semua produk untuk penggunaan parenteral, larutan yang telah diencerkan dan larutan infus TAXOTERE mesti diperiksa secara visual sebelum digunakan, larutan yang mengandung endapan mesti dibuang.
5. KAEDAH PENGHILANGAN
Semua alat yang telah digunakan untuk mencairkan atau mengelola TAXOTERE harus dirawat sesuai dengan prosedur standard. Jangan membuang ubat ke saluran pembuangan. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
CUKAI 20 MG / 0,5 ML
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap botol dos tunggal TAXOTERE 20 mg / 0.5 ml pekat yang mengandungi docetaxel dalam bentuk trihydrate, sepadan dengan 20 mg docetaxel (anhydrous). Larutan likat mengandungi 40 mg / ml docetaxel (anhidrat).
Eksipien: Setiap botol pelarut dos tunggal mengandungi 13% (b / b) 95% etanol dalam air untuk suntikan.
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI
Pekat dan pelarut untuk larutan untuk infusi.
Pekat adalah larutan jernih, likat, kuning hingga kuning-coklat.
Pelarut adalah larutan tidak berwarna.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Kanser payudara:
TAXOTERE dalam kombinasi dengan doxorubicin dan cyclophosphamide ditunjukkan untuk rawatan tambahan pesakit dengan:
- kanser payudara positif kelenjar getah bening yang dapat dikendalikan;
- barah payudara negatif yang boleh dikendalikan.
Pada pesakit dengan barah payudara negatif yang boleh dikendalikan, rawatan adjuvan harus dibatasi kepada pesakit yang merupakan calon kemoterapi mengikut kriteria antarabangsa untuk rawatan barah payudara peringkat awal. (lihat bahagian 5.1).
TAXOTERE dalam kombinasi dengan doxorubicin ditunjukkan untuk rawatan pesakit dengan barah payudara maju atau metastatik tempatan yang belum pernah menerima terapi sitotoksik sebelumnya untuk penyakit ini.
TAXOTERE sebagai monoterapi ditunjukkan untuk rawatan pesakit dengan barah payudara maju atau metastatik tempatan setelah kegagalan terapi sitotoksik. Kemoterapi sebelumnya mesti mengandungi agen anthracycline atau alkylating.
TAXOTERE dalam kombinasi dengan trastuzumab ditunjukkan untuk rawatan pesakit dengan barah payudara metastatik dengan ekspresi berlebihan HER2 dan yang sebelumnya tidak pernah menerima kemoterapi untuk penyakit metastatik.
TAXOTERE dalam kombinasi dengan capecitabine ditunjukkan untuk rawatan pesakit dengan barah payudara maju atau metastatik tempatan setelah kegagalan kemoterapi sitotoksik.
Kemoterapi sebelumnya mesti merangkumi anthracycline. Kanser paru-paru sel bukan kecil TAXOTERE ditunjukkan untuk rawatan pesakit dengan barah paru-paru sel kecil atau metastatik yang maju selepas kegagalan kemoterapi sebelumnya.
TAXOTERE dalam kombinasi dengan cisplatin ditunjukkan untuk rawatan pesakit dengan barah paru-paru sel kecil yang tidak dapat dirawat, maju atau metastatik yang tidak pernah mendapat kemoterapi sebelumnya untuk keadaan ini.
Kanser prostat:
TAXOTERE dalam kombinasi dengan prednisone atau prednisolone ditunjukkan untuk rawatan pesakit dengan kanser prostat metastatik refraktori hormon.
Adenokarsinoma gastrik:
TAXOTERE dalam kombinasi dengan cisplatin dan 5-fluorouracil ditunjukkan untuk rawatan pesakit dengan adenokarsinoma gastrik metastatik, termasuk adenokarsinoma persimpangan gastroesofagus, yang sebelumnya tidak pernah menerima kemoterapi untuk penyakit metastatik mereka.
Kanser kepala dan leher:
TAXOTERE dalam kombinasi dengan cisplatin dan 5-fluorouracil ditunjukkan untuk rawatan induksi pada pesakit dengan karsinoma sel skuamosa maju dan kepala.
04.2 Posologi dan kaedah pentadbiran
Penggunaan docetaxel harus terhad kepada jabatan yang khusus dalam pentadbiran terapi sitotoksik dan pentadbirannya harus di bawah pengawasan doktor yang pakar dalam penggunaan kemoterapi antikanker (lihat bahagian 6.6).
Dos yang disyorkan:
Untuk barah payudara, barah paru-paru sel kecil, adenokarsinoma gastrik dan barah kepala dan leher, premedikasi dengan kortikosteroid oral seperti dexamethasone 16 mg / hari (mis. 8 mg BID) selama 3 hari bermula 1 hari sebelum pentadbiran docetaxel (lihat bahagian 4.4) Profilaksis G-CSF dapat digunakan untuk mengurangkan risiko keracunan hematologi.
Untuk barah prostat, memandangkan penggunaan prednisone atau prednisolon bersamaan, ubat yang disyorkan adalah oral dexamethasone 8 mg 12 jam, 3 jam dan 1 jam sebelum infus docetaxel (lihat bahagian 4.4).
Docetaxel diberikan sebagai infus satu jam setiap tiga minggu.
Kanser payudara:
Untuk terapi pelengkap barah payudara positif dan urat simpul negatif, dos docetaxel yang disyorkan adalah 75 mg / m2 diberikan 1 jam selepas doxorubicin 50 mg / m2 dan siklofosfamid 500 mg / m2 setiap 3 minggu selama 6-kitaran. (TAC rejimen ) (lihat juga Penyesuaian dos semasa rawatan).
Untuk rawatan pesakit dengan barah payudara maju atau metastatik, dos monoterapi docetaxel yang disyorkan adalah 100 mg / m2. Dalam rawatan lini pertama, docetaxel 75 mg / m2 diberikan bersama dengan doxorubicin (50 mg / m2).
Dalam kombinasi dengan trastuzumab, dos docetaxel yang disyorkan adalah 100 mg / m2 setiap 3 minggu, dengan trastuzumab diberikan setiap minggu. Dalam kajian penting, infus docetaxel awal dimulakan sehari selepas pemberian trastuzumab pertama. Dos docetaxel berikutnya diberikan segera setelah infus trastuzumab jika dos trastuzumab sebelumnya dapat diterima dengan baik. Untuk dos dan pentadbiran trastuzumab lihat ringkasan ciri produk untuk trastuzumab.
Dalam kombinasi dengan capecitabine, dos docetaxel yang disyorkan adalah 75 mg / m2 setiap tiga minggu, bersama dengan capecitabine pada dos 1250 mg / m2 dua kali sehari (dalam 30 minit selepas makan) selama 2 minggu diikuti dengan selang 1 minggu . Untuk pengiraan dos capecitabine mengikut luas permukaan badan, lihat ringkasan ciri produk capecitabine.
Kanser paru-paru sel tidak kecil:
Pada pesakit yang tidak pernah menerima kemoterapi untuk kanser paru-paru sel kecil, dos yang disyorkan adalah docetaxel 75 mg / m2 diikuti dengan segera oleh cisplatin 75 mg / m2 selama 30-60 minit. Untuk rawatan setelah kegagalan kemoterapi yang mengandungi platinum sebelumnya, dos yang disyorkan adalah 75 mg / m2 sebagai monoterapi.
Kanser prostat:
Dos docetaxel yang disyorkan ialah 75 mg / m2. Prednisone atau prednisolone 5 mg secara lisan dua kali sehari diberikan selama tempoh rawatan (lihat bahagian 5.1).
Adenokarsinoma gastrik:
Dos docetaxel yang disyorkan adalah 75 mg / m2 sebagai infus 1 jam, diikuti oleh cisplatin 75 mg / m2, sebagai infus 1 - 3 jam (kedua-duanya pada hari pertama sahaja), diikuti oleh 5-fluorouracil 750 mg. / M2 per hari diberikan sebagai infus 24 jam berterusan selama 5 hari, bermula dari akhir infus cisplatin. Rawatan diulang setiap tiga minggu. Pesakit harus mendapat ubat awal dengan antiemetik dan penghidratan yang mencukupi untuk penggunaan cisplatin.
Profilaksis G-CSF harus digunakan untuk mengurangkan risiko keracunan hematologi (lihat juga Penyesuaian dos semasa rawatan).
Kanser kepala dan leher:
Pesakit harus mendapat ubat antiemetik pra-ubat dan penghidratan yang mencukupi (sebelum dan sesudah pemberian cisplatin). Profilaksis G-CSF dapat dilakukan sedemikian rupa untuk mengurangkan risiko keracunan hematologi. Semua pesakit yang menjalani rawatan docetaxel kajian TAX 323 dan TAX 324 diterima profilaksis antibiotik.
Kemoterapi induksi diikuti dengan radioterapi (CUKAI 323):
Untuk rawatan induksi pada pesakit dengan karsinoma sel skuamosa yang tidak dapat dikendalikan secara tempatan (SCCHN), dos docetaxel yang disyorkan adalah 75 mg / m2 sebagai infus 1 jam diikuti dengan 75 mg / m2 cisplatin selama lebih dari 1 jam, pada hari 1, diikuti dengan 5-fluorouracil 750 mg / m2 sehari yang diberikan sebagai infus 24 jam berterusan selama 5 hari. Jadual dos ini diberikan setiap 3 minggu selama 4 kitaran. Selepas kemoterapi, pesakit mesti menerima radioterapi.
Kemoterapi induksi diikuti dengan kemoradioterapi (CUKAI 324):
Untuk rawatan induksi pesakit dengan karsinoma sel skuamosa maju dan kepala (SCCHN) (secara teknikal tidak dapat dijalankan, dengan kebarangkalian kejayaan pembedahan yang rendah, dan dengan tujuan untuk pemeliharaan organ) dos docetaxel yang disyorkan adalah 75 mg / m2 sebagai infus 1 jam pada hari ke-1, diikuti oleh cisplatin 100 mg / m2 diberikan sebagai infus yang berlangsung 30 minit hingga tiga jam, diikuti oleh 5-fluorouracil 1000 mg / m2 setiap hari, diberikan dalam infus berterusan 1 - 4 hari. Jadual dos ini diberikan setiap tiga minggu selama tiga kitaran. Selepas kemoterapi, pesakit harus menerima kemoterapi.
Untuk pengubahsuaian dos 5-fluorouracil dan cisplatin, lihat Ringkasan Karakteristik Produk tertentu. Penyesuaian dos semasa rawatan:
Am
Docetaxel harus diberikan apabila jumlah neutrofil adalah 3 1500 sel / mm3.
Pada pesakit yang mengalami neutropenia demam, neuropati periferal neutrofil teruk semasa terapi docetaxel, dos docetaxel harus dikurangkan dari 100 mg / m2 hingga 75 mg / m2 dan / atau dari 75 hingga 60 mg / m2. Sekiranya, pada 60 mg / m2, pesakit terus mengalami reaksi ini, rawatan harus dihentikan.
Terapi tambahan untuk barah payudara:
Profilaksis G-CSF primer harus dipertimbangkan untuk pesakit yang menerima terapi adjuvan dengan docetaxel, doxorubicin dan cyclophosphamide (TAC) untuk barah payudara. Pada pesakit yang mengalami jangkitan neutropenia demam dan / atau jangkitan neutropenik, dos docetaxel harus dikurangkan menjadi 60 mg / m2 dalam semua kursus berikutnya (lihat bahagian 4.4 dan 4.8). Pada pesakit yang mengalami stomatitis Gred 3 atau 4 dos harus dikurangkan menjadi 60 mg / m2
Berkaitan dengan cisplatin:
Bagi pesakit yang awalnya dirawat dengan docetaxel 75 mg / m2 dalam kombinasi dengan cisplatin dan jumlah platelet nadir dalam terapi sebelumnya adalah
Dalam kombinasi dengan capecitabine:
Untuk penyesuaian dos capecitabine, lihat Ringkasan Karakteristik Produk untuk capecitabine.
Pada pesakit yang mengalami penampilan pertama keracunan Gred 2 yang berterusan pada masa pemberian docetaxel / capecitabine berikutnya, rawatan harus ditangguhkan sehingga disahkan ke Gred 0-1, dan kemudian disambung semula pada 100% dari dos permulaan.
Pada pesakit yang mengalami kejadian ketoksikan Gred 2 yang kedua, atau kejadian keracunan Gred 3 yang pertama pada mana-mana tahap terapi, rawatan harus ditangguhkan sehingga resolusi ke Gred 0-1, dan kemudian dilanjutkan dengan docetaxel 55 mg / m2 .
Untuk sebarang kejadian keracunan atau ketoksikan Gred 4, hentikan terapi docetaxel.
Untuk pengubahsuaian dos trastuzumab, lihat Ringkasan Karakteristik Produk untuk trastuzumab.
Berkaitan dengan cisplatin dan 5-fluorouracil:
Sekiranya episod neutropenia demam, neutropenia berpanjangan atau neutropenia jangkitan berlaku walaupun penggunaan G-CSF, dos docetaxel harus dikurangkan dari 75 hingga 60 mg / m2. Sekiranya episod neutropenia rumit selanjutnya, dos docetaxel harus dikurangkan dari 60 hingga 45 mg / m2. Untuk trombositopenia Gred 4, dos docetaxel harus dikurangkan dari 75 hingga 60 mg / m2. Pesakit tidak boleh dirawat dengan kursus docetaxel lebih lanjut sehingga neutrofil kembali ke tahap> 1,500 sel / mm3 dan platelet kembali ke tahap> 100,000 sel / mm3. Hentikan rawatan jika ketoksikan ini berterusan (lihat bahagian 4.4). Perubahan dos yang disyorkan kerana ketoksikan pada pesakit yang dirawat dengan docetaxel dalam kombinasi dengan cisplatin dan 5-fluorouracil (5-FU):
Untuk pengubahsuaian dos cisplatin dan 5-fluorouracil, lihat Ringkasan Karakteristik Produk tertentu.
Dalam kajian penting SCCHN pada pesakit yang mengalami neutropenia rumit (termasuk neutropenia berpanjangan, neutropenia demam, atau jangkitan), penggunaan GCSF disarankan untuk memberikan liputan profilaksis (misalnya, hari 6-15) dalam semua kitaran berikutnya.
Populasi khas:
Pesakit dengan kekurangan hepatik:
Berdasarkan data farmakokinetik dengan docetaxel pada 100 mg / m2 diberikan sebagai rawatan tunggal, pada pesakit dengan peningkatan transaminase (ALT dan / atau AST) lebih besar daripada 1.5 kali had atas fosfatase normal dan alkali lebih besar daripada 2.5 kali had atas normal , dos docetaxel yang disyorkan ialah 75 mg / m2 (lihat bahagian 4.4 dan 5.2). Bagi pesakit dengan bilirubin serum melebihi had atas normal dan / atau ALT dan AST> 3,5 kali had atas normal yang berkaitan dengan alkali fosfatase lebih besar daripada 6 kali had atas normal, tidak ada pengurangan dos yang disyorkan dan docetaxel tidak akan melakukannya mesti diberikan kecuali dalam keadaan yang dinyatakan dengan tegas.
Dalam kombinasi dengan cisplatin dan 5-fluorouracil untuk rawatan pesakit dengan adenokarsinoma gastrik, kajian klinikal penting mengecualikan pesakit dengan ALT dan / atau AST> 1.5 kali had atas normal yang dikaitkan dengan nilai fosfatase alkali.> 2.5 kali had atas normal dan pada nilai bilirubin> 1 kali had atas normal; untuk pesakit ini, pengurangan dos tidak boleh disarankan dan docetaxel tidak boleh digunakan kecuali dinyatakan dengan tegas. Tidak ada data yang tersedia pada pesakit dengan gangguan hati yang dirawat dengan docetaxel dalam kombinasi dalam petunjuk lain.
Populasi kanak-kanak:
Keselamatan dan keberkesanan TAXOTERE dalam barah nasofaring pada kanak-kanak berumur 1 bulan hingga kurang dari 18 tahun belum terbukti.
Tidak ada data mengenai penggunaan TAXOTERE pada populasi pediatrik dalam indikasi barah payudara, barah paru-paru sel kecil, barah prostat, barah gastrik dan barah kepala dan leher, tidak termasuk kanser nasofaring jenis II dan III yang kurang dibezakan.
Warga emas.
Berdasarkan farmakokinetik populasi, tidak ada arahan khas untuk digunakan pada orang tua.
Dalam kombinasi dengan capecitabine untuk pesakit berusia 60 tahun dan lebih tua, pengurangan dos permulaan hingga 75% disyorkan (lihat Ringkasan Karakteristik Produk untuk capecitabine).
04.3 Kontraindikasi
Hipersensitiviti terhadap bahan aktif atau mana-mana eksipien.
Docetaxel tidak boleh digunakan pada pesakit dengan jumlah neutrofil awal
Docetaxel tidak boleh digunakan pada pasien dengan gangguan hati yang teruk kerana kekurangan data yang tersedia (lihat bahagian 4.2 dan 4.4).
Kontraindikasi untuk ubat lain juga berlaku ketika digunakan dalam kombinasi dengan docetaxel.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
Kecuali dikontraindikasikan, pra-ubat dengan kortikosteroid oral, seperti dexamethasone 16 mg setiap hari (contohnya 8 mg BID) selama 3 hari, bermula sehari sebelum pentadbiran docetaxel, selama 3 hari bermula sehari sebelum pentadbiran docetaxel untuk kanser paru-paru sel dan payudara kecil, dapat mengurangkan "kejadian dan keparahan penahanan cecair serta keparahan reaksi hipersensitiviti. Untuk kanser prostat, premedikasi adalah oral dexamethasone 8 mg, 12 jam, 3 jam dan 1 jam sebelum infus docetaxel (lihat perenggan 4.2).
Hematologi:
Neutropenia adalah tindak balas buruk yang paling kerap diperhatikan dengan docetaxel. Neutrofil nadir muncul selepas 7 hari (nilai median) tetapi pada pesakit yang banyak dirawat selang ini mungkin dipendekkan. Pemeriksaan jumlah darah yang lengkap harus dilakukan dengan kerap pada semua pesakit yang menerima docetaxel.
Sekiranya neutropenia teruk (
Pada pesakit yang dirawat dengan docetaxel bersama dengan cisplatin dan 5-fluorouracil (TCF), neutropenia demam dan jangkitan neutropenik berlaku dengan kejadian yang lebih rendah ketika pesakit menerima profilaksis G-CSF. Pesakit yang dirawat dengan TCF harus menerima G-CSF sebagai profilaksis untuk mengurangkan risiko neutropenia yang rumit (neutropenia demam, neutropenia yang berpanjangan, atau jangkitan neutropenik). Pesakit yang menerima TCF harus dipantau dengan teliti (lihat bahagian 4.2 dan 4.8).
Pada pesakit yang dirawat dengan docetaxel dalam kombinasi dengan doxorubicin dan cyclophosphamide (rejimen TAC), neutropenia demam dan / atau jangkitan neutropenik terjadi dengan "kejadian yang lebih rendah ketika pesakit menerima profilaksis G-CSF primer. Profilaksis G-CSF primer. CSF harus dipertimbangkan pada pasien menerima terapi CT adjuvan untuk barah payudara untuk mengurangkan risiko neutropenia rumit (neutropenia demam, neutropenia berpanjangan atau jangkitan neutropenik). Pesakit yang menerima imbasan CT harus dipantau dengan teliti (lihat bahagian 4.2 dan 4.8).
Reaksi hipersensitiviti:
Pesakit harus dipantau dengan teliti untuk kemungkinan berlakunya reaksi hipersensitiviti, terutama semasa infusi pertama dan kedua. Reaksi hipersensitiviti mungkin berlaku dalam beberapa minit selepas memulakan infus docetaxel oleh itu perlu ada cara untuk merawat hipotensi dan bronkospasme. Sekiranya reaksi hipersensitiviti dengan gejala kecil seperti kemerahan atau reaksi kulit setempat berlaku, tidak perlu menghentikan terapi. Walau bagaimanapun, reaksi yang teruk, seperti hipotensi teruk, bronkospasme atau ruam / eritema umum memerlukan penghentian segera infus docetaxel dan rawatan yang sesuai. Pesakit yang mengalami reaksi hipersensitiviti yang teruk tidak boleh lagi mengambil docetaxel.
Reaksi kulit:
Eritema kulit setempat di hujung kaki (telapak tangan dan telapak kaki) dengan edema diikuti dengan desquamation telah diperhatikan. Gejala teruk seperti ruam diikuti dengan pengelupasan yang menyebabkan penghentian rawatan docetaxel sementara atau kekal telah dilaporkan (lihat bahagian 4.2).
Pengekalan cecair:
Pesakit dengan pengekalan cecair yang teruk, seperti efusi pleura, perikardium dan asites, harus dipantau dengan teliti.
Pesakit dengan disfungsi hepatik:
Pada pesakit yang dirawat dengan docetaxel pada kadar 100 mg / m2 sahaja yang mempunyai kadar transaminase serum (ALT dan / atau AST) lebih besar daripada 1.5 kali had atas normal bersamaan dengan tahap fosfatase alkali serum lebih besar daripada 2.5 kali had atas normal, c "berisiko tinggi mendapat reaksi buruk yang serius seperti kematian toksik termasuk sepsis gastrointestinal dan pendarahan yang boleh membawa maut, neutropenia demam, jangkitan, trombositopenia, stomatitis dan asthenia. Oleh itu, pada pesakit dengan fungsi fungsi hati tinggi, dos docetaxel yang disyorkan adalah 75 mg / m2 dan ujian fungsi hati harus dilakukan sebelum memulakan rawatan dan sebelum setiap kitaran (lihat bahagian 4.2).
Pada pesakit yang mempunyai nilai bilirubin serum lebih besar daripada had atas normal dan / atau nilai ALT dan AST lebih besar daripada 3.5 kali had atas normal dengan alkali fosfatase lebih tinggi daripada 6 kali had atas normal, pengurangan dos tidak boleh disyorkan. dan docetaxel tidak boleh digunakan kecuali dinyatakan dengan tegas.
Dalam kombinasi dengan cisplatin dan 5-fluorouracil untuk rawatan pesakit dengan adenokarsinoma gastrik, kajian klinikal penting mengecualikan pesakit dengan ALT dan / atau AST> 1.5 kali had atas normal yang dikaitkan dengan nilai fosfatase alkali.> 2.5 kali had atas normal dan pada nilai bilirubin> 1 kali had atas normal; untuk pesakit ini, pengurangan dos tidak dapat disarankan dan docetaxel tidak boleh digunakan kecuali dinyatakan dengan tegas.
Pesakit dengan fungsi buah pinggang terjejas:
Tidak ada data yang tersedia pada pesakit dengan gangguan ginjal yang teruk yang menerima terapi docetaxel.
Sistem saraf:
Kejadian neurotoksisiti periferal yang teruk memerlukan pengurangan dos (lihat bahagian 4.2).
Ketoksikan jantung:
Kegagalan jantung telah diperhatikan pada pesakit yang dirawat dengan docetaxel dalam kombinasi dengan trastuzumab, terutama setelah kemoterapi yang mengandungi anthracyclines (doxorubicin atau epirubicin).
Ini didapati sederhana hingga teruk dan dikaitkan dengan kematian (lihat bahagian 4.8).
Apabila pesakit adalah calon docetaxel secara kontrasuzumab, mereka harus menjalani penilaian jantung asas. Fungsi jantung harus dipantau lebih lanjut selama rawatan (mis. Setiap tiga bulan) untuk mengenal pasti pesakit yang mungkin mengalami kelainan jantung. Lihat ringkasan ciri produk untuk trastuzumab untuk maklumat lebih lanjut.
Yang lain:
Langkah-langkah kontraseptif harus digunakan selama rawatan untuk lelaki dan wanita dan untuk lelaki sekurang-kurangnya enam bulan setelah penghentiannya (lihat bahagian 4.6).
Langkah berjaga-jaga tambahan untuk rawatan barah payudara
Neutropenia yang rumit:
Bagi pesakit yang mengalami neutropenia rumit (neutropenia berpanjangan, neutropenia demam atau jangkitan), terapi G-CSF dan pengurangan dos harus dipertimbangkan (lihat bahagian 4.2).
Kejadian gastrousus:
Gejala seperti sakit perut dan malaise, demam, cirit-birit dengan atau tanpa neutropenia, boleh menjadi manifestasi awal keracunan gastrointestinal yang teruk dan harus dinilai dan dirawat dengan segera.
Kegagalan jantung kongestif:
Pesakit harus ditindaklanjuti untuk gejala yang boleh menyebabkan kegagalan jantung kongestif semasa terapi dan tempoh tindak lanjut.
Leukemia:
Pada pesakit yang dirawat dengan docetaxel, doxorubicin dan cyclophosphamide (TAC) risiko myelodysplasia tertunda atau myeloid leukemia memerlukan tindak lanjut hematologi.
Pesakit dengan 4 atau lebih kelenjar getah bening positif:
Keseimbangan manfaat-risiko terapi CT pada pesakit dengan 4 atau lebih kelenjar getah bening positif tidak sepenuhnya ditentukan dengan analisis sementara (lihat bahagian 5.1).
Warga emas:
Data terhad tersedia pada pesakit berusia lebih dari 70 tahun yang dirawat dengan docetaxel dalam kombinasi dengan doxorubicin dan cyclophosphamide.
Dalam kajian kanser prostat terhadap 333 pesakit yang dirawat dengan docetaxel setiap tiga minggu, 209 berumur 65 tahun atau lebih tua dan 68 pesakit berusia lebih dari 75 tahun. Pada pesakit yang dirawat dengan docetaxel setiap tiga minggu, kejadian perubahan plat kuku yang berkaitan dengan ubat, pada pesakit yang berumur 65 tahun ke atas, lebih tinggi daripada 10% berbanding pesakit yang lebih muda. Kejadian demam yang berkaitan dengan ubat, cirit-birit, anoreksia dan edema periferal pada pesakit berusia 75 tahun ke atas lebih daripada 10% lebih tinggi daripada pada pesakit di bawah 65 tahun.
Di antara 300 pesakit (221 dalam kajian fasa III dan 79 dalam kajian fasa II) dirawat dengan docetaxel dalam kombinasi dengan cisplatin dan 5-fluorouracil dalam kajian barah gastrik, 74 adalah 65 atau lebih tua dan 4 daripadanya 75 atau lebih tua. Kejadian kejadian buruk serius pada orang tua berbanding pesakit yang lebih muda.Kesan kejadian buruk lebih tinggi pada orang tua berbanding pesakit muda. Kejadian kejadian buruk berikut (semua peringkat): kelesuan, stomatitis, dan jangkitan neutropenik berlaku dengan kekerapan> 10% pada pesakit 65 tahun ke atas berbanding pesakit yang lebih muda. Pesakit tua yang dirawat dengan TCF harus dipantau dengan sangat berhati-hati.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Kajian in vitro telah menunjukkan bahawa metabolisme docetaxel dapat diubah dengan pemberian sebatian yang bersamaan yang mendorong atau menghambat sitokrom P450-3A atau yang dimetabolisme olehnya (dan oleh itu dapat menghambat enzim secara kompetitif), seperti siklosporin, terfenadine, ketoconazole , eritromisin dan troleandomisin Oleh itu, berhati-hati harus diberikan semasa merawat pesakit bersamaan dengan produk ubat tersebut kerana potensi risiko interaksi penting.
Docetaxel sangat terikat protein (> 95%). Walaupun kemungkinan interaksi in vivo antara docetaxel dan terapi bersamaan belum diselidiki secara khusus, interaksi in vitro antara ubat-ubatan yang terikat protein seperti eritromisin, diphenhydramine, propranolol, propafenone, phenytoin, salicylates, sulfamethoxazole dan sodium valproate tidak mempengaruhi pengikatan docetaxel kepada protein. Tambahan pula, dexamethasone tidak mengubah pengikatan protein docetaxel. Docetaxel tidak mempengaruhi pengikatan digitoxin.Farmakokinetik docetaxel, doxorubicin dan cyclophosphamide tidak mengganggu semasa mereka bersama. Data terhad dari satu kajian yang tidak terkawal nampaknya menunjukkan interaksi antara docetaxel dan carboplatin. Apabila digunakan dalam kombinasi dengan docetaxel, pelepasan karboplatin kira-kira 50% lebih tinggi daripada nilai yang dilaporkan sebelumnya untuk digunakan sendiri.
Farmakokinetik docetaxel dengan kehadiran prednison dikaji pada pesakit dengan kanser prostat metastatik. Docetaxel dimetabolisme oleh CYP3A4 dan prednison menyebabkan induksi CYP3A4. Tidak ada kesan statistik prednisone yang signifikan terhadap farmakokinetik docetaxel.
Docetaxel harus diberikan dengan berhati-hati kepada pesakit yang secara bersamaan mengambil perencat CYP3A4 yang kuat (contohnya perencat protease seperti ritonavir, antifungal azole seperti ketoconazole atau itraconazole). Kajian interaksi ubat yang dilakukan pada pesakit yang mengambil ketoconazole dan docetaxel menunjukkan bahawa pelepasan docetaxel dikurangkan separuh kerana ketoconazole, mungkin kerana metabolisme docetaxel melibatkan CYP3A4 sebagai jalur metabolik yang dominan. Toleransi terganggu terhadap docetaxel mungkin berlaku, walaupun pada dos rendah.
04.6 Kehamilan dan penyusuan
Tidak ada maklumat mengenai penggunaan docetaxel pada wanita hamil. Dalam kajian pada tikus dan arnab, docetaxel adalah embriooksik dan foetotoksik dan mengurangkan kesuburan pada tikus. Seperti produk ubat sitotoksik lain, docetaxel boleh menyebabkan kemudaratan janin apabila diberikan kepada wanita hamil. alasan docetaxel tidak boleh diberikan kepada wanita hamil kecuali dinyatakan dengan jelas.
Wanita usia subur / kontrasepsi:
Wanita berpotensi melahirkan anak yang dirawat dengan docetaxel harus dinasihatkan untuk menghindari risiko kehamilan dan segera memberitahu doktor mereka jika ini terjadi.
Kaedah kontrasepsi yang berkesan harus digunakan semasa rawatan.
Dalam kajian bukan klinikal, docetaxel mempunyai kesan genotoksik dan boleh menjejaskan kesuburan lelaki (lihat bahagian 5.3). Oleh itu, lelaki yang dirawat dengan docetaxel dianjurkan untuk tidak membiak selama dan hingga 6 bulan setelah rawatan dan bertanya tentang penyimpanan sperma sebelum rawatan.
Masa makan:
Docetaxel adalah bahan lipofilik tetapi tidak diketahui sama ada ia diekskresikan dalam susu manusia. Oleh itu, memandangkan potensi reaksi buruk pada bayi, penyusuan susu ibu harus dihentikan semasa rawatan docetaxel.
04.7 Kesan terhadap kemampuan memandu dan menggunakan mesin
Tidak ada kajian mengenai kesan keupayaan memandu atau menggunakan mesin yang dilakukan.
04.8 Kesan yang tidak diingini
Reaksi buruk yang dianggap mungkin atau mungkin berkaitan dengan pentadbiran docetaxel diperoleh dalam:
1312 dan 121 pesakit yang masing-masing menerima docetaxel 100 mg / m2 dan 75 mg / m2 sebagai monoterapi.
258 pesakit yang menerima docetaxel dalam kombinasi dengan doxorubicin.
406 pesakit yang menerima docetaxel dalam kombinasi dengan cisplatin.
92 pesakit dirawat docetaxel dalam kombinasi dengan trastuzumab.
255 pesakit yang menerima docetaxel dalam kombinasi dengan capecitabine.
332 pesakit yang menerima docetaxel dalam kombinasi dengan prednisone atau prednisolone (kesan yang tidak diingini berkaitan dengan rawatan klinikal ditunjukkan).
1276 pesakit (masing-masing 744 dan 532 dalam CUKAI 316 dan GEICAM 9805) yang menerima docetaxel dalam kombinasi dengan doxorubicin dan siklofosfamid (kesan yang tidak diingini berkaitan dengan rawatan berkaitan klinikal ditunjukkan).
300 pesakit adenokarsinoma gastrik (221 dalam kajian fasa III dan 79 dalam kajian fasa II) dirawat dengan docetaxel dalam kombinasi dengan cisplatin dan 5-fluorouracil (berlaku kesan tidak diingini yang berkaitan dengan rawatan penting secara klinikal).
174 pesakit dengan barah kepala dan leher dirawat dengan docetaxel bersama dengan cisplatin dan 5-fluorouracil (kesan sampingan yang penting secara klinikal berkaitan dengan rawatan telah berlaku).
Reaksi ini telah dijelaskan dengan Kriteria Ketoksikan Biasa NCI (gred 3 = G3; gred 3- -4 = G3 / 4; gred 4 = G4) dan dengan istilah COSTART dan MedDRA. Kekerapan ditakrifkan sebagai:
sangat biasa (≥ 1/10); biasa (≥ 1/100 hingga
Dalam setiap kelas frekuensi, kesan yang tidak diingini dilaporkan mengikut tahap keparahan yang menurun.
Reaksi buruk yang paling kerap dilaporkan semasa penggunaan docetaxel sahaja adalah: neutropenia (reversibel dan tidak terkumpul; hari rata-rata hingga nadir adalah hari ke-7 dan tempoh purata neutropenia teruk (anemia, alopecia, mual, muntah, stomatitis, cirit-birit dan asthenia) kejadian buruk docetaxel mungkin meningkat apabila docetaxel diberikan bersama dengan agen kemoterapi lain.
Untuk kombinasi dengan trastuzumab, kejadian buruk (semua nilai) dilaporkan sebagai peratusan 10%. Terdapat peningkatan kejadian kejadian buruk yang serius (40% lwn 31%) dan kejadian buruk kelas 4 (34% lwn 23%) dalam kumpulan kombinasi trastuzumab berbanding monoterapi docetaxel. Untuk kombinasi dengan capecitabine, kesan yang tidak diingini berkaitan dengan rawatan yang paling kerap (≥ 5%) yang diperhatikan dalam kajian klinikal fasa III pada pesakit barah payudara setelah kegagalan terapi anthracycline dilaporkan (lihat ringkasan ciri produk. Capecitabine).
Reaksi buruk berikut sering diperhatikan dengan docetaxel:
Gangguan sistem imun:
Reaksi hipersensitiviti biasanya berlaku dalam beberapa minit selepas memulakan infus docetaxel dan pada amnya ringan hingga sederhana. Gejala yang paling kerap dilaporkan adalah kilat panas, ruam dengan atau tanpa gatal, sesak dada, sakit belakang, dyspnoea, dan demam atau menggigil. Reaksi teruk dicirikan oleh hipotensi dan / atau bronkospasme atau ruam / eritema umum (lihat bahagian 4.4)
Gangguan sistem saraf:
Perkembangan neurotoksisiti periferal yang teruk memerlukan pengurangan dos (lihat bahagian 4.2 dan 4.4).
Tanda-tanda sensorineural ringan hingga sederhana dicirikan oleh paraesthesia, disesthesia atau kesakitan termasuk pembakaran. Kejadian neuromotor dicirikan terutamanya oleh kelemahan.
Gangguan tisu kulit dan subkutan:
Reaksi kulit yang boleh dipulihkan telah diperhatikan dan umumnya dianggap ringan hingga sederhana. Reaksi dicirikan oleh ruam, termasuk letusan setempat terutamanya di kaki dan tangan (termasuk sindrom kaki-tangan yang teruk), tetapi juga di lengan, muka atau dada, yang sering dikaitkan dengan pruritus. Letusan secara amnya berlaku dalam satu minggu dari infus docetaxel. Gejala yang lebih jarang seperti letusan diikuti dengan desquamation telah dilaporkan yang jarang memerlukan penghentian sementara atau kekal rawatan (lihat bahagian 4.2 dan 4.4). Gejala serius telah dilaporkan. Perubahan kuku ditandai dengan hipopigmentasi atau hiperpigmentasi, kadang-kadang sakit dan onikolisis.
Gangguan umum dan keadaan tapak pentadbiran:
Reaksi di tempat infusi pada umumnya ringan dan dicirikan oleh hiperpigmentasi, keradangan, kemerahan dan kekeringan pada kulit, phlebitis atau extravasation, "peningkatan kebolehtelapan" urat.
Pengekalan cecair yang merangkumi kes edema periferal dan jarang berlaku kes pleura, efusi perikardial, asites dan kenaikan berat badan. Edema periferal biasanya berlaku bermula di bahagian bawah kaki dan boleh menjadi umum dengan kenaikan berat badan sebanyak 3 kg atau lebih.Penahan cecair adalah kumulatif dalam kejadian dan intensiti (lihat bahagian 4.4).
TAXOTERE 100 mg / m2 sebagai monoterapi
Gangguan sistem darah dan limfa
Jarang: episod pendarahan yang berkaitan dengan trombositopenia kelas 3/4.
Gangguan sistem saraf
Data kebolehbalikan tersedia pada 35.3% pesakit yang mengalami neurotoksisitas berikutan rawatan dengan monoterapi docetaxel 100 mg / m2. Kejadian itu dapat dipulihkan secara spontan dalam masa 3 bulan.
Gangguan tisu kulit dan subkutan
Sangat jarang berlaku: satu kes alopecia yang tidak boleh ditarik balik pada akhir kajian. 73% reaksi kulit dapat diterbalikkan dalam masa 21 hari.
Gangguan umum dan keadaan tapak pentadbiran
Purata dos kumulatif pada pemberhentian rawatan adalah lebih dari 1,000 mg / m2 dan masa median untuk kebolehbalikan pengekalan cecair adalah 16.4 minggu (antara 0 hingga 42 minggu). Permulaan pengekalan sederhana hingga teruk (min dos kumulatif: 818.9 mg / m2) ditangguhkan pada pesakit yang menerima premedikasi berbanding pesakit tanpa premedikasi (min dos kumulatif: 489.7 mg / m2); namun, pada beberapa pesakit, telah dilaporkan semasa menjalani terapi pertama.
TAXOTERE 75 mg / m2 sebagai monoterapi
TAXOTERE 75 mg / m2 dalam kombinasi dengan doxorubicin
TAXOTERE 75 mg / m2 dalam kombinasi dengan cisplatin
TAXOTERE 100 mg / m2 dalam kombinasi dengan trastuzumab
Patologi jantung
Gagal jantung simptomatik dilaporkan pada 2.2% pesakit yang menerima docetaxel dalam kombinasi dengan trastuzumab, dibandingkan dengan 0% pesakit yang menerima docetaxel sahaja. Dalam kumpulan docetaxel dan trastuzumab, 64% pesakit sebelumnya telah menerima anthracyclines sebagai terapi tambahan berbanding dengan 55% pesakit yang dirawat dengan docetaxel sahaja.
Gangguan sistem darah dan limfa
Sangat biasa: Ketoksikan hematologi meningkat pada pesakit yang dirawat dengan trastuzumab dan docetaxel berbanding dengan yang dirawat dengan docetaxel sahaja (kelas 3/4 neutropenia 32% berbanding 22% mengikut kriteria NCI-CTC). Perhatikan bahawa ini mungkin terlalu rendah kerana docetaxel sahaja pada dos 100 mg / m2 diketahui menyebabkan neutropenia pada 97% pesakit, kelas 4 dalam 76%, berdasarkan nadir jumlah neutrofil. Kejadian neutropenia demam / sepsis neutropenik juga meningkat pada pesakit yang dirawat dengan Herceptin dan docetaxel (23% berbanding 17% pesakit yang dirawat dengan docetaxel sahaja).
TAXOTERE 75 mg / m2 dalam kombinasi dengan capecitabine
TAXOTERE 75 mg / m2 dalam kombinasi dengan prednisone atau prednisolone
Terapi tambahan dengan TAXOTERE 75 mg / m2 dalam kombinasi dengan doxorubicin dan cyclophosphamide pada pesakit dengan barah payudara positif (TAX 316) dan barah payudara negatif (GEICAM 9805) - data kumulatif:
Gangguan sistem saraf
Semasa tindak lanjut, 12 daripada 83 pesakit yang pernah mengalami neuropati deria periferi pada akhir kemoterapi masih mengalami gejala neuropati deria periferal.
Patologi jantung
Kegagalan jantung kongestif (CHF) dilaporkan pada 18 dari 1276 pesakit dalam tempoh susulan. Dalam kajian positif-simpul (TAX316) satu pesakit dalam setiap kumpulan rawatan meninggal dunia akibat kegagalan jantung.
Gangguan tisu kulit dan subkutan
Semasa tindak lanjut, 25 daripada 736 pesakit yang mengalami alopecia pada akhir kemoterapi masih mengalami alopecia.
Penyakit sistem pembiakan dan payudara
Semasa tindak lanjut, 140 daripada 251 pesakit yang mengalami amenore pada akhir kemoterapi masih mengalami gejala amenorea.
Gangguan umum dan keadaan tapak pentadbiran
Semasa tindak lanjut, 18 dari 112 pesakit yang mengalami edema periferal pada akhir kemoterapi dalam kajian TAX 316 masih mengalami gejala edema periferal, sementara 4 dari 5 pesakit yang mengalami limfedema pada akhir kemoterapi pada GEICAM 9805 masih mengalami gejala edema periferal. gejala limfedema.
Sindrom Leukemia Akut / Myelodysplastic.
Pada tindak lanjut rata-rata 77 bulan, leukemia akut terjadi pada 1 dari 532 (0.2%) pesakit yang menerima docetaxel, doxorubicin dan cyclophosphamide pada GEICAM 9805. Tidak ada kes yang dilaporkan pada pasien yang menerima fluorouracil., Doxorubicin dan cyclophosphamide. Tidak ada kes sindrom myelodysplastic yang didiagnosis pada mana-mana kumpulan rawatan. Jadual di bawah menunjukkan bahawa kejadian neutropenia Gred 4, neutropenia demam dan jangkitan neutropenik dikurangkan pada pesakit yang mendapat profilaksis G-CSF primer setelah menjadi wajib dalam kajian TAC - kajian GEICAM.
Komplikasi Neutropenik pada pesakit yang mendapat CT dengan atau tanpa profilaksis G-CSF primer (GEICAM 9805)
TAXOTERE 75 mg / m2 dalam kombinasi dengan cisplatin dan 5-fluorouracil untuk adenokarsinoma gastrik
Gangguan sistem darah dan limfa
Neutropenia demam dan jangkitan neutropenik berlaku pada 17.2% dan 13.5% pesakit, tanpa mengira penggunaan G-CSF. G-CSF digunakan untuk profilaksis sekunder pada 19.3% pesakit (10.7% kursus). Neutropenia demam dan jangkitan neutropenik masing-masing berlaku pada 12.1% dan 3.4% pesakit yang menerima G-CSF sebagai profilaksis, pada 15.6% dan 12.9% pesakit tanpa profilaksis dengan G-CSF (lihat bahagian 4.2).
TAXOTERE 75 mg / m2 dalam kombinasi dengan cisplatin dan 5-fluorouracil untuk kanser kepala dan leher
Kemoterapi induksi diikuti dengan radioterapi (CUKAI 323)
Kemoterapi induksi diikuti dengan radioterapi kemo (TAX324)
Pengalaman pasca pemasaran:
Neoplasma jinak, ganas dan tidak ditentukan (termasuk sista dan polip)
Kes leukemia myeloid akut dan sindrom myelodysplastic yang sangat jarang berlaku apabila docetaxel digunakan bersama dengan agen kemoterapi dan / atau radioterapeutik lain.
Gangguan sistem darah dan limfa
Penindasan sumsum tulang dan reaksi buruk hematologi lain telah dilaporkan. Pembekuan intravaskular yang disebarkan telah sering dilaporkan berkaitan dengan sepsis atau kegagalan pelbagai organ.
Gangguan sistem imun
Beberapa kes kejutan anafilaksis, beberapa yang membawa maut, telah dilaporkan.
Gangguan sistem saraf
Kes sawan yang jarang berlaku atau kehilangan kesedaran sementara telah diperhatikan berikutan pemberian docetaxel. Reaksi ini kadang-kadang muncul semasa infusi.
Gangguan mata
Kes perubahan visual yang jarang berlaku (kilatan, kilatan cahaya, scotoma) dan berkaitan dengan reaksi hipersensitiviti biasanya berlaku semasa penyerapan produk ubat. Ini telah dapat dibalikkan setelah penghentian infus. Kes-kes lakrimasi dengan atau tanpa konjungtivitis jarang dilaporkan, seperti kes penyumbatan saluran air mata akibat terkoyak berlebihan.
Gangguan telinga dan labirin
Kes ototoksisiti, gangguan pendengaran dan / atau gangguan pendengaran jarang dilaporkan.
Patologi jantung
Kes infark miokard jarang berlaku.
Patologi vaskular
Kejadian tromboemboli vena jarang dilaporkan.
Gangguan pernafasan, toraks dan mediastinum
Sindrom gangguan pernafasan akut, pneumonia interstisial dan fibrosis paru jarang dilaporkan. Kes-kes jarang pneumonia akibat radiasi telah dilaporkan pada pesakit yang juga menjalani terapi radiasi.
Gangguan saluran gastrousus
Episod dehidrasi yang jarang dilaporkan sebagai akibat gangguan gastrointestinal, perforasi gastrointestinal, kolitis iskemia, kolitis dan enterokolitis neutropenik. Kes jarang berlaku penyumbatan ileal dan usus.
Gangguan hepatobiliari
Kes hepatitis yang sangat jarang berlaku, kadang-kadang membawa maut, dilaporkan terutama pada pesakit dengan penyakit hati yang sudah ada sebelumnya.
Gangguan tisu kulit dan subkutan
Kes dari lupus eritematosus letusan kulit dan bulosa seperti eritema multiforme, sindrom Stevens-Johnson, nekrolisis epidermis toksik. Dalam beberapa kes, faktor bersamaan lain mungkin menyumbang kepada perkembangan kesan ini. Manifestasi seperti Schleroderma biasanya didahului oleh limfedema periferal telah dilaporkan semasa rawatan dengan docetaxel.
Gangguan umum dan keadaan tapak pentadbiran
Fenomena penarikan sinaran jarang dilaporkan.
Pengekalan cecair tidak dikaitkan dengan episod akut oliguria atau hipotensi. Dehidrasi dan edema paru jarang dilaporkan.
04.9 Overdosis
Beberapa kes overdosis telah dilaporkan. Tidak ada penawar yang diketahui untuk overdosis docetaxel. Sekiranya berlaku overdosis, pesakit harus disimpan dalam unit khusus dan fungsi penting diawasi dengan teliti.Jika berlaku overdosis, dapat terjadi peningkatan kejadian buruk. Komplikasi utama yang diharapkan dalam overdosis adalah penekanan sumsum tulang, neurotoksisiti periferal dan mukositis. Pesakit harus menerima terapi G-CSF secepat mungkin setelah bukti berlebihan. Langkah-langkah simptomatik lain yang sesuai harus diambil sekiranya diperlukan.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapi: tekana, kod ATC: L01CD 02
Data praklinikal:
Docetaxel adalah ubat antineoplastik yang bertindak dengan mempromosikan agregasi tubulin menjadi mikrotubulus stabil dan menghalang pemecahannya, sehingga menyebabkan penurunan ketara dalam tubulin bebas. Pengikatan docetaxel ke mikrotubulus tidak mengubah jumlah protofilamen. secara in vitro ia memecah sistem mikrotubular selular yang penting untuk fungsi sel penting seperti mitosis dan interphase.
The docetaxel secara in vitro sitotoksik terhadap pelbagai garis tumor tikus dan manusia dan tumor manusia yang baru dikeluarkan dalam ujian klonogenik yang dijalankan. Docetaxel mencapai kepekatan intra-selular yang tinggi dan tahan lama. Selanjutnya docetaxel aktif pada beberapa barisan sel (tetapi tidak semua) yang mengekspresikan kelebihan p-glikoprotein, yang dikodkan oleh gen tahan pelbagai ubat. Dalam vivo, docetaxel secara eksperimen mempunyai spektrum tindakan yang luas terhadap tumor murine maju dan tumor manusia yang dicangkokkan, tanpa mengira rejimen dos.
Data klinikal:
Kanser payudara
TAXOTERE dalam kombinasi dengan doxorubicin dan cyclophosphamide: rawatan adjuvan.
Pesakit dengan barah payudara positif nod yang dapat dikendalikan (CUKAI 316)
Data dari kajian multisenter berlabel terbuka yang menyokong penggunaan docetaxel sebagai rawatan tambahan pada pesakit dengan barah payudara positif urat simpul dan KPS 3 80% berumur 18 hingga 70 tahun. Berikutan stratifikasi berdasarkan bilangan kelenjar getah bening positif (1-3 , lebih daripada 4), 1491 pesakit secara rawak menerima docetaxel 75 mg / m2 yang diberikan 1 jam selepas doxorubicin 50 mg / m2 dan cyclophosphamide 500 mg / m2 (kumpulan TAC) atau doxorubicin 50 mg / m2 diikuti dari fluorouracil 500 mg / m2 dan siklofosfamid 500 mg / m2 (kumpulan FAC). Kedua-dua rejimen diberikan sekali setiap 3 minggu selama 6 kitaran. Docetaxel diberikan sebagai infus 1 jam, semua produk ubat lain diberikan sebagai bolus intravena pada hari 1. G-CSF diberikan sebagai profilaksis sekunder kepada pesakit dengan neutropenia rumit (neutropenia demam, neutropenia atau jangkitan berpanjangan).
Pesakit dalam kumpulan TAC menerima profilaksis antibiotik dengan ciprofloxacin 500 mg oral atau antibiotik setara dua kali sehari selama 10 hari bermula pada hari ke-5 setiap kitaran. Dalam kedua-dua kumpulan, setelah menjalani kemoterapi terakhir, pesakit positif reseptor estrogen dan / atau progestogen menerima tamoxifen 20 mg / hari selama 5 tahun. Terapi radiasi tambahan diresepkan mengikut panduan yang berlaku di setiap pusat yang mengambil bahagian dan ia diberikan kepada 69 % pesakit yang menerima TAC dan hingga 72% pesakit yang menerima FAC.
Analisis sementara dilakukan pada masa tindak lanjut rata-rata 55 bulan. Kelangsungan hidup bebas penyakit meningkat dengan ketara pada kumpulan TAC berbanding dengan kumpulan FAC.
Kejadian kambuh 5 tahun dikurangkan pada pesakit yang menerima TAC berbanding dengan mereka yang menerima FAC (masing-masing 25% vs 32%) iaitu penurunan risiko mutlak sebanyak 7% (p = 0.001). Keseluruhan kelangsungan hidup pada 5 tahun juga ketara meningkat dengan TAC berbanding FAC (masing-masing 87% vs 81%) iaitu pengurangan risiko kematian secara mutlak 6% (p = 0,008). Subkumpulan pesakit yang dirawat dengan TAC sesuai dengan faktor prognostik utama yang ditentukan a priori dianalisis:
* nisbah bahaya kurang dari 1 menunjukkan bahawa TAC dikaitkan dengan kelangsungan hidup bebas penyakit dan kelangsungan hidup keseluruhan lebih tinggi daripada FAC
Pada analisis sementara, kelebihan terapi TAC pada pesakit dengan 4 atau lebih kelenjar getah bening (37% daripada populasi) tidak ditunjukkan. Kelebihan terapi TAC nampaknya kurang jelas daripada yang diperhatikan pada pesakit dengan 1 hingga 3 limfa positif Nisbah risiko / faedah, oleh itu, pada pesakit dengan 4 atau lebih kelenjar getah bening positif tidak ditentukan sepenuhnya pada peringkat analisis ini.
Pesakit dengan calon barah payudara negatif yang boleh dikendalikan untuk kemoterapi (GEICAM 9805):
Data dari kajian multisenter, terbuka dan rawak menyokong penggunaan TAXOTERE untuk terapi adjuvan pada pesakit dengan barah payudara negatif-operasi yang merupakan calon kemoterapi. 1060 pesakit secara rawak menerima TAXOTERE 75 mg / m2 yang diberikan 1 jam selepas doxorubicin. 50 mg / m2 dan siklofosfamid 500 mg / m2 (539 pesakit di lengan TAC), atau doxorubicin 50 mg / m2 diikuti oleh fluorouracil 500 mg / m2 dan siklofosfamid 500 mg / m2 (521 pesakit di lengan FAC) sebagai terapi tambahan dalam barah kelenjar getah bening negatif payudara yang dapat dikendalikan dengan risiko tinggi kambuh mengikut kriteria St. Gallen 1998 (ukuran tumor> 2 cm dan / atau ER dan PR negatif dan / atau tahap histologi / nuklear tinggi (gred 2 hingga 3) dan / atau umur
Tempoh masa tindak lanjut adalah 77 bulan. Peningkatan yang signifikan secara statistik dalam kelangsungan hidup bebas penyakit ditunjukkan untuk lengan TAC berbanding dengan lengan FAC. Pesakit yang dirawat dengan TAC mempunyai pengurangan 32% risiko kambuh dibandingkan dengan pesakit yang dirawat dengan FAC (nisbah bahaya = 0,68, 95% CI (0,49-0,93), p = 0,01). Keseluruhan kelangsungan hidup (OS) juga lebih lama di lengan TAC dengan pengurangan risiko kematian 24% bagi pesakit yang dirawat dengan TAC berbanding FAC (nisbah bahaya = 0,76, 95% CI (0,46-1, 26, p = 0,29) Walau bagaimanapun, pengagihan kelangsungan hidup secara keseluruhan tidak berbeza antara kedua-dua kumpulan.
Subkumpulan pesakit yang dirawat dengan TAC dianalisis dibahagikan mengikut faktor prognostik utama yang ditentukan secara prospektif (lihat jadual di bawah):
Analisis Subkumpulan - Kajian Terapi Adjuvant pada Pesakit dengan Kanser Payudara Node-Negatif (Analisis Intent-to-Treat)
* nisbah bahaya (TAC / FAC) kurang dari 1 menunjukkan bahawa TAC dikaitkan dengan kelangsungan hidup bebas penyakit yang lebih lama daripada FAC.
Analisis subkumpulan eksploratif untuk kelangsungan hidup bebas penyakit pada pesakit yang memenuhi kriteria St. Gallen 2009 untuk kemoterapi - (populasi ITT) telah dilakukan dan ditunjukkan dalam jadual di bawah:
TAC = docetaxel, doxorubicin dan siklofosfamid
FAC = 5-fluorouracil, doxorubicin dan siklofosfamid
CI = selang keyakinan; ER = reseptor estrogen
PR = reseptor progesteron
ER / PR negatif atau Gred 3 atau saiz tumor> 5 cm
Nisbah bahaya dianggarkan dengan model bahaya berkadar Cox menggunakan kumpulan terapi sebagai faktor.
TAXOTERE sebagai satu-satunya rawatan
Dua kajian perbandingan rawak fasa III dengan docetaxel pada dos yang disyorkan dan rejimen 100 mg / m2 setiap 3 minggu dilakukan pada pesakit dengan barah payudara metastatik, di mana 326 selepas kegagalan rawatan alkilasi dan 392 setelah kegagalan. Rawatan dengan antrasiklin.
Pada pesakit di mana rawatan dengan agen alkilasi didapati tidak berkesan, docetaxel dibandingkan dengan doxorubicin (75 mg / m2 setiap 3 minggu). Docetaxel meningkatkan kadar tindak balas (52% berbanding 37%, p = 0.01) dan menurunkan masa tindak balas (12 minggu berbanding 23 minggu, p = 0.007), tanpa mengubah masa bertahan (15 bulan untuk docetaxel berbanding 14 bulan untuk doxorubicin, p = 0.38) atau masa untuk kemajuan (27 minggu untuk docetaxel berbanding 23 minggu untuk doxorubicin, p = 0.54). Tiga pesakit yang dirawat docetaxel (2%) terpaksa menghentikan rawatan kerana pengekalan cairan, sementara 15 pesakit yang dirawat doxorubicin (9%) terpaksa berhenti kerana ketoksikan jantung (tiga kematian akibat kegagalan jantung kongestif).
Pada pesakit yang rawatan antrasiklinnya tidak berkesan, docetaxel dibandingkan dengan kombinasi mitomycin C dan vinblastine (12 mg / m2 setiap 6 minggu dan 6 mg / m2 setiap 3 minggu). Docetaxel meningkatkan kadar tindak balas (33% berbanding 12%, h
Profil toleransi docetaxel selama dua fasa III kajian ini sesuai dengan profil toleransi yang terdapat dalam kajian fasa II (lihat bahagian 4.8).
Kajian Fasa III multisenter secara rawak, terbuka yang membandingkan monoterapi docetaxel dengan paclitaxel dilakukan dalam rawatan barah payudara lanjut pada pesakit yang terapi sebelumnya sudah termasuk "anthracycline. Sebanyak 449 pesakit secara rawak untuk menerima salah satu monoterapi docetaxel 100 mg / m2 sebagai infus 1 jam atau paclitaxel 175 mg / m2 sebagai infus 3 jam, kedua rawatan tersebut diberikan setiap 3 minggu.
Docetaxel memanjangkan jangka masa median hingga kemajuan (24.6 minggu berbanding 15.6 minggu; h
TAXOTERE dalam kombinasi dengan doxorubicin
Kajian fasa III secara rawak telah dilakukan pada 429 pesakit dengan kanser metastatik yang tidak diobati membandingkan doxorubicin (50 mg / m2) dalam kombinasi dengan docetaxel (75 mg / m2) (lengan AT) dengan doxorubicin (60 mg / m2). Dalam kombinasi dengan siklofosfamid (600 mg / m2) (lengan AC). Kedua-dua rejimen diberikan pada hari pertama setiap tiga minggu.
Masa untuk kemajuan (TTP) meningkat dengan ketara pada lengan AT berbanding dengan lengan AC, p = 0,0138. TTP median adalah 37.3 minggu (95% CI: 33.4 - 42.1) di lengan AT dan 31.9 minggu (95% CI: 27.4 - 36.0) di lengan AC.
Kadar tindak balas yang diperhatikan jauh lebih tinggi pada lengan AT berbanding dengan lengan AC, p = 0,009. Kadar ini adalah 59.3% (95% CI: 52.8 - 65.9) pada lengan AT berbanding 46.5% (95% CI: 39.8 - 53.2) pada lengan AC.
Dalam kajian ini, lengan AT mempunyai kejadian yang lebih tinggi daripada lengan AC neutropenia teruk (90% vs 68.6%), neutropenia demam (33.3% vs 10%), jangkitan (8% vs 2.4%), cirit-birit (7.5% vs 1.4%), asthenia (8.5% vs 2.4%), dan kesakitan (2.8% vs 0%). Sebaliknya, lengan AC menunjukkan kejadian anemia yang lebih tinggi daripada lengan AT (15.8% berbanding 8.5%) dan kejadian ketoksikan jantung yang lebih tinggi: kegagalan jantung kongestif (3.8% berbanding 2, 8%), penurunan mutlak dalam LVEF 3 20% (13.1% vs 6.1%), penurunan mutlak dalam LVEF ≥ 30% (6.2% vs 1.1%). Kematian beracun berlaku pada 1 pesakit di lengan AT (kegagalan jantung kongestif) dan pada 4 pesakit di lengan AC (1 disebabkan oleh kejutan septik dan 3 disebabkan oleh kegagalan jantung kongestif).
Di kedua-dua lengan, kualiti hidup, diukur dengan soal selidik EORTC, dapat dibandingkan dan stabil semasa rawatan dan tindak lanjut.
TAXOTERE dalam kombinasi dengan trastuzumab
Docetaxel dalam kombinasi dengan trastuzumab telah dinilai dalam perawatan pasien dengan barah payudara metastatik yang terlalu banyak menyatakan HER2 dan yang belum pernah menerima kemoterapi sebelumnya untuk penyakit metastatik. 186 pesakit secara rawak menerima docetaxel (100 mg / m2) dengan atau tanpa trastuzumab; 60% pesakit sebelum ini menerima kemoterapi adjuvan dengan anthracyclines. Docetaxel dengan trastuzumab berkesan pada pesakit yang telah atau tidak pernah menerima terapi anthracycline tambahan. Ujian yang paling biasa digunakan untuk menentukan positif HER2 dalam kajian penting ini adalah imunohistokimia (IHC). Fluoresensi in situ assay (FISH) digunakan untuk sebilangan kecil pesakit.Dalam kajian ini 87% pesakit mempunyai penyakit IHC 3+ dan 95% pesakit yang mendaftar mempunyai penyakit IHC 3+ dan / atau IKAN positif. Hasil keberkesanan dirangkum dalam jadual di bawah:
TTP = masa untuk kemajuan; "ne" menunjukkan bahawa ia tidak dapat diperkirakan atau belum
dicapai.
1 Populasi yang ingin dirawat
2 Dianggarkan kelangsungan hidup median
TAXOTERE dalam kombinasi dengan capecitabine
Data dari percubaan klinikal fasa III multisentra, rawak, terkawal menyokong penggunaan docetaxel dalam kombinasi dengan capecitabine untuk rawatan pesakit dengan kanser payudara maju atau metastatik selepas kegagalan kemoterapi sitotoksik yang merangkumi anthracycline. Dalam kajian ini, 255 pesakit secara rawak menjalani rawatan dengan docetaxel (75 mg / m2 sebagai infus intravena 1 jam setiap 3 minggu) dan capecitabine (1250 mg / m2 dua kali sehari selama 2 minggu diikuti dengan waktu rehat 1 minggu.). 256 pesakit secara rawak menjalani rawatan dengan docetaxel sahaja (100 mg / m2 sebagai infus intravena selama 1 jam setiap 3 minggu). Kelangsungan hidup lebih unggul di lengan kombinasi docetaxel + capecitabine (p = 0.0126). Kelangsungan hidup median adalah 442 hari (docetaxel + capecitabine) berbanding dengan 352 hari (docetaxel sahaja). Tahap tindak balas objektif keseluruhan di seluruh populasi secara rawak (penilaian penyiasat) adalah 41.6% (docetaxel + capecitabine) berbanding 29.7% (docetaxel sahaja); p = 0.0058. Masa untuk perkembangan penyakit adalah lebih baik pada lengan kombinasi docetaxel + capecitabine (p
Kanser paru-paru sel tidak kecil
Pesakit sebelum ini dirawat dengan kemoterapi dengan atau tanpa radioterapi
Dalam kajian klinikal fasa III, pada pesakit yang dirawat sebelumnya, masa untuk perkembangan (12.3 minggu vs 7 minggu) dan kelangsungan hidup meningkat dengan ketara dengan docetaxel pada 75 mg / m2 berbanding dengan Rawatan Sokongan Terbaik (MTS).
Kadar kelangsungan hidup 1 tahun jauh lebih tinggi dengan docetaxel (40%) berbanding dengan MTS (16%).
Lebih sedikit morfin digunakan pada pesakit yang dirawat dengan docetaxel pada 75 mg / m2 (p analgesik bukan morfin (p
Pada pesakit yang dapat dinilai, kadar tindak balas keseluruhan adalah 6.8%, dan jangka masa purata tindak balas adalah 26.1 minggu.
TAXOTERE dalam kombinasi dengan derivatif platinum pada pesakit yang tidak pernah dirawat dengan kemoterapi
Dalam kajian fasa III, 1218 pesakit dengan barah sel sel kecil IIIB atau IV yang tidak dapat dikendalikan, dengan Status Prestasi Karnofsky 70% ke atas, yang tidak pernah menerima kemoterapi sebelumnya untuk keadaan ini, secara rawak ke docetaxel (T) 75 mg / m2 sebagai infusi satu jam diikuti dengan segera oleh cisplatin (TCis) 75 mg / m2 selama 30-60 minit setiap tiga minggu, docetaxel 75 mg / m2 sebagai infusi satu jam dalam kombinasi dengan karboplatin (AUC 6 mg / ml. min) lebih dari 30-60 minit setiap tiga minggu, atau vinorelbine (VCis) 25 mg / m2 diberikan selama 6-10 minit pada hari 1, 8, 15, 22 diikuti oleh cisplatin 100 mg / m2 diberikan pada hari pertama kitaran diulang setiap 4 minggu.
Kelangsungan hidup, waktu min untuk kemajuan dan data kadar tindak balas untuk dua kumpulan kajian ditunjukkan dalam jadual di bawah.
*: Dibetulkan untuk beberapa perbandingan dan disesuaikan untuk faktor stratifikasi (peringkat penyakit dan kawasan rawatan), berdasarkan populasi pesakit yang dapat dinilai.
Titik akhir sekunder termasuk perubahan kesakitan, penilaian kualiti hidup global oleh EuroQoL-5D, Skala Gejala Kanser Paru-Paru (LCSS), dan perubahan status prestasi Karnofsky. Hasil objektif ini mengesahkan hasil objektif utama.
Untuk kombinasi docetaxel / carboplatin, tidak mungkin menunjukkan kesetaraan atau tidak rendahnya keberkesanan berkenaan dengan rawatan rujukan: kombinasi VCis.
Kanser prostat
Toleransi dan keberkesanan docetaxel dalam kombinasi dengan prednisone atau prednisolone pada pesakit dengan kanser prostat metastatik refraktori hormon dinilai dalam kajian rawak multisentra fasa III. Sebanyak 1006 pesakit dengan KPS 60 secara rawak ke kumpulan terapi berikut:
Docetaxel 75 mg / m2 setiap 3 minggu selama 10 kitaran.
Docetaxel 30 mg / m2 diberikan setiap minggu untuk 5 minggu pertama kitaran 6 minggu untuk jumlah 5 kitaran.
Mitoxantrone 12 mg / m2 setiap 3 minggu selama 10 kitaran.
Ketiga-tiga rejimen diberikan bersama dengan prednison atau prednisolon 5 mg dua kali sehari, secara berterusan.
Pesakit yang menerima docetaxel setiap tiga minggu menunjukkan kelangsungan hidup keseluruhan yang jauh lebih lama daripada pesakit yang dirawat dengan mitoxantrone. Peningkatan kelangsungan hidup yang diperhatikan dalam kumpulan yang dirawat docetaxel setiap minggu tidak signifikan secara statistik berbanding dengan kumpulan kawalan yang dirawat dengan mitoxantrone. Parameter keberkesanan yang diperoleh dalam kumpulan yang dirawat docetaxel dibandingkan dengan kumpulan kawalan diringkaskan dalam jadual berikut:
† Ujian peringkat log berstrata
* Had untuk kepentingan statistik = 0.0175
** PSA: Antigen Khusus Prostat
Oleh kerana docetaxel setiap minggu mempunyai profil toleransi yang sedikit lebih baik daripada docetaxel setiap 3 minggu, ada kemungkinan beberapa pesakit mendapat manfaat daripada terapi docetaxel mingguan.
Tidak ada perbezaan yang signifikan secara statistik dalam Keseluruhan Kualiti Hidup antara kumpulan rawatan.
Adenokarsinoma gastrik
Kajian multicentre, randomized, open-label dilakukan untuk menilai keselamatan dan keberkesanan docetaxel dalam rawatan pesakit dengan adenokarsinoma gastrik metastatik, termasuk adenokarsinoma persimpangan gastroesofagus, yang sebelumnya tidak menerima kemoterapi untuk penyakit metastatik mereka. Sebanyak 445 pesakit dengan KPS> 70 dirawat docetaxel (T) (75 mg / m2 pada hari ke-1) dalam kombinasi dengan cisplatin (C) (75 mg / m2 pada hari 1) dan 5-fluorouracil (F) (750 mg / m2 sehari selama 5 hari) atau dengan cisplatin (100 mg / m2 pada hari 1) dan 5-fluorouracil (1000 mg / m2 sehari selama 5 hari). Tempoh kitaran rawatan adalah 3 minggu untuk lengan TCF dan 4 minggu untuk lengan CF. Purata bilangan kitaran yang diberikan bagi setiap pesakit adalah 6 (dengan jarak 1-16) untuk lengan TCF dan 4 (dengan jarak 1-12) untuk lengan CF. Masa untuk kemajuan (TTP) adalah titik akhir utama. Pengurangan risiko perkembangan adalah 32.1% dan dikaitkan dengan TTP yang jauh lebih lama (p = 0.0004) untuk lengan TCF. Keseluruhan kelangsungan hidup juga jauh lebih lama (p = 0.0201) untuk bahagian TCF dengan risiko penurunan kematian sebanyak 22.7%. Hasil keberkesanan diringkaskan dalam jadual berikut:
Keberkesanan docetaxel dalam rawatan pesakit dengan adenokarsinoma gastrik
* Ujian logrank tidak berstrata
Analisis subkumpulan untuk usia, jantina, dan bangsa secara konsisten memilih lengan TCF berbanding lengan CF.
Analisis kelangsungan hidup yang dikemas kini yang dilakukan dengan masa tindak lanjut rata-rata 41.6 bulan tidak lagi menunjukkan perbezaan yang signifikan secara statistik, walaupun selalu memihak kepada rejimen TCF dan menekankan bahawa manfaat TCF berbanding CF jelas. Antara 18 dan 30 bulan mengikuti -kepada.
Secara keseluruhan, kualiti hidup (QoL) dan hasil manfaat klinikal secara konsisten menunjukkan peningkatan yang memihak kepada TCF. Pesakit yang dirawat dengan TCF mempunyai masa 5% lebih lama untuk kemerosotan status kesihatan pada soal selidik QLQ-C30 (p = 0,0121) dan masa yang lebih lama untuk kemerosotan definisi status prestasi Karnofsky (p = 0, 0088) berbanding dengan pesakit yang dirawat dengan CF .
Kanser kepala dan leher
Kemoterapi induksi diikuti dengan radioterapi (CUKAI 323)
Keselamatan dan keberkesanan docetaxel dalam rawatan induksi pesakit dengan karsinoma sel skuamosa kepala dan leher (SCCHN) dinilai dalam kajian rawak fasa III berlabel terbuka (TAX323). Dalam kajian ini, 358- pesakit dengan tempatan maju SCCHN yang tidak dapat dikendalikan dengan status prestasi WHO 0 - 1 secara rawak dari satu hingga dua lengan. Pesakit yang menerima docetaxel (T) 75 mg / m2 diikuti oleh cisplatin (P) 75 mg / m2 diikuti oleh 5- fluorouracil (F) 750 mg / m2 setiap hari sebagai infus berterusan selama 5 hari Rejimen dos ini diberikan setiap tiga minggu selama 4 kitaran, tindak balas minimum (pengecutan tumor> 25% diukur dalam dua dimensi) diperhatikan selepas 2 kitaran. Pada akhir kemoterapi, dengan selang minimum 4 minggu dan maksimum tujuh minggu, pesakit yang penyakitnya tidak berkembang menerima radioterapi (RT), sesuai dengan panduan institusi, selama 7 minggu. dan (TPF / RT). Pesakit di lengan pembanding menerima cisplatin (P) 100 mg / m2 diikuti oleh 5-fluorouracil (F) 1000 mg / m2 setiap hari selama 5 hari. Rejimen dos ini diberikan setiap tiga minggu selama 4 kitaran jika sekurang-kurangnya satu tindak balas (penurunan tumor 25% dalam ukuran tumor dua dimensi yang diukur) diperhatikan setelah 2 siklus. Pada kesimpulan kemoterapi, dengan selang minimum 4 minggu dan selang maksimum 7 minggu, pesakit di mana penyakit itu belum berkembang menerima radioterapi (RT) sesuai dengan panduan selama 7 minggu (PF / RT). Terapi radiasi lokoregional diterapkan pada pecahan konvensional (1,8 Gy-2,0 Gy sekali sehari, 5 hari seminggu untuk jumlah dos 66 hingga 70 Gy), atau untuk rejimen radioterapi dipercepat / hiperfraksinasi (dua kali sehari, dengan selang minimum pecahan 6 jam, 5 hari seminggu). Sebanyak 70 Gy dicadangkan untuk rejimen dipercepat dan 74 Gy untuk skema hiperfraksi. Reseksi pembedahan dibenarkan selepas kemoterapi, sebelum atau selepas radioterapi. Pesakit di lengan TPF menerima ciprofloxacin oral 500 mg dua kali sehari selama 10 hari bermula pada hari ke-5 setiap kitaran, atau setara, sebagai profilaksis. Titik akhir utama dalam kajian ini, kelangsungan hidup bebas kemajuan (PFS), jauh lebih lama di lengan TPF daripada di lengan PF, p = 0.0042 (PFS median: 11.4 vs 8.3 bulan, masing-masing) dengan masa median 33.7 bulan. kelangsungan hidup juga jauh lebih lama untuk lengan TPF berbanding PF (median OS: masing-masing 18.6 vs 14.5 bulan) dengan penurunan risiko kematian sebanyak 28%, p = 0.0128. Hasil keberkesanan ditunjukkan dalam jadual di bawah:
Keberkesanan docetaxel dalam rawatan induksi pesakit dengan SCCHN yang tidak dapat dioperasikan secara tempatan. (Analisis Intent-to-Treat).
Nisbah bahaya lebih rendah daripada 1 yang menyokong gabungan docetaxel + cisplatin + 5-FU
* Model Cox (penyesuaian untuk tapak tumor primer, pementasan pada T dan N dan PS-WHO)
** Ujian Logrank
*** Ujian Chi-square
Parameter untuk menentukan kualiti hidup.
Pesakit yang dirawat dengan TPF menunjukkan penurunan kesihatan keseluruhan mereka secara signifikan berbanding pesakit yang dirawat dengan PF (p = 0.01, menggunakan skala EORTC QLQ-C30).
Parameter untuk menentukan faedah klinikal
Skala prestasi, untuk kepala dan leher (PSS-HN), yang bertujuan untuk mengukur pemahaman ucapan, kemungkinan makan di tempat umum dan normalnya diet, didapati secara signifikan memihak pada lengan TPF berbanding dengan lengan PF . Masa median hingga kemerosotan pertama dalam keadaan prestasi WHO jauh lebih lama di lengan TPF berbanding dengan lengan PF. Skala intensiti kesakitan menunjukkan peningkatan semasa rawatan di kedua-dua kumpulan, menunjukkan bahawa pengurusan kesakitan mencukupi.
Kemoterapi induksi diikuti dengan kemoterapi-radioterapi (TAX324)
Keselamatan dan keberkesanan docetaxel dalam rawatan induksi pesakit dengan karsinoma sel skuamosa kepala dan leher (SCCHN) yang maju secara tempatan dinilai dalam percubaan klinikal fasa III, rawak, label terbuka, multisenter (TAX 324). Kajian, 501 pesakit dengan SCCHN maju tempatan dengan status prestasi WHO 0 atau 1 secara rawak ke salah satu daripada dua lengan. Populasi kajian juga merangkumi pesakit yang tidak dapat dikendalikan secara teknikal, pesakit dengan kebarangkalian yang rendah untuk berjaya menjalani pembedahan, dan pesakit yang bertujuan untuk pemuliharaan organ. profil keselamatan dan keberkesanan dianggap hanya titik akhir kelangsungan hidup, sedangkan kejayaan dalam pemuliharaan organ tidak dipertimbangkan secara formal.
Pesakit yang dirawat Docetaxel menerima docetaxel (T) 75 mg / m2 sebagai infus intravena pada hari 1 diikuti oleh cisplatin (P) 100 mg / m2 diberikan sebagai infus intravena yang berlangsung 30 minit hingga tiga jam, diikuti dengan infus intravena berterusan 5- fluorouracil (F) 1000 mg / m2 / hari dari hari 1 hingga hari 4. Kitaran diulang setiap tiga minggu selama 3 kitaran.
Semua pesakit yang tidak mengalami perkembangan penyakit harus menerima kemoterapi radioterapi (CRT) sesuai protokol (TPF / CRT). Pesakit di bahagian pembanding menerima cisplatin (P) 100 mg / m2 yang diberikan sebagai infus yang berlangsung dari 30 minit hingga tiga jam pada hari 1, diikuti oleh 5-fluorouracil (F) 1000 mg / m2 / hari dari hari 1 hingga hari. Siklus diulang setiap tiga minggu selama 3 kitaran. Semua pesakit yang tidak mengalami perkembangan penyakit harus menerima CRT patuh protokol (PF / CRT).
Pesakit di kedua lengan rawatan menerima CRT selama 7 hari selepas kemoterapi induksi dengan selang minimum 3 minggu dan tidak lebih dari 8 minggu selepas permulaan kitaran terakhir (hari ke 22 hingga hari ke 56. Semasa radioterapi, karboplatin (AUC 1.5) diberikan sebagai infus intravena selama satu jam sehingga 7 dos. Sinaran diberikan dengan instrumen voltan tinggi menggunakan pecahan harian (2Gy sehari, 5 hari seminggu selama 7 minggu, dengan jumlah dos 70-72 Gy). Pembedahan di lokasi tumor primer dan / atau leher dapat dipertimbangkan setiap saat setelah selesai CRT. Semua pesakit kajian di lengan docetaxel mendapat profilaksis antibiotik. Titik akhir keberkesanan utama kajian ini, kelangsungan hidup (OS) jauh lebih lama (ujian peringkat log p = 0.0058) dengan rejimen yang mengandung docetaxel berbanding PF (OS median: 70.6 vs 30.1 bulan, masing-masing), dengan pengurangan 30% dalam risiko kematian akibat PF (nisbah bahaya (HP) = 0,70, selang keyakinan 95% (CI) = 0,54-0,90) pada tindak lanjut rata-rata 41,9 bulan Titik akhir sekunder, PFS, menunjukkan penurunan 29% dalam risiko kemajuan atau kematian dan peningkatan PFS median 22 bulan (35.5 bulan untuk TPF dan 13.1 untuk PF). Ini juga signifikan secara statistik dengan HR 0.71, 95% CI 0.56-0.90; log-rank test p = 0.004. Hasil keberkesanan ditunjukkan dalam jadual berikut:
Nisbah bahaya lebih rendah daripada 1 yang menyokong gabungan docetaxel + cisplatin + 5-fluorouracil
* penyesuaian ujian peringkat log
** penyesuaian ujian peringkat log, tidak ada penyesuaian untuk pelbagai perbandingan
*** Ujian Chi-square, tidak ada penyesuaian untuk pelbagai perbandingan
NA - tidak berkenaan
Agensi Ubat-ubatan Eropah telah memberikan pengecualian dari kewajiban untuk memberikan hasil kajian dengan TAXOTERE di semua subkumpulan pesakit populasi pediatrik dalam barah payudara, barah paru-paru sel kecil, barah prostat, barah gastrik dan barah kepala dan leher, tidak termasuk karsinoma nasofaring jenis II dan jenis III yang kurang dibezakan (lihat bahagian 4.2 untuk maklumat mengenai penggunaan pediatrik).
05.2 "Sifat farmakokinetik
Farmakokinetik docetaxel dikaji pada pesakit barah setelah pemberian 20-115 mg / m2 dalam kajian fasa I. Profil kinetik docetaxel tidak bergantung pada dos dan konsisten dengan model farmakokinetik tiga petak, dengan separuh hayat per fasa a, b dan b masing-masing 4 min, 36 min. dan 11.1 jam. Fasa akhir sebahagiannya disebabkan oleh pemulangan docetaxel yang agak perlahan dari petak periferal. Setelah pemberian 100 mg / m2 sebagai infus satu jam, rata-rata tahap plasma puncak 3.7 mcg / ml diperoleh, dengan AUC yang sepadan 4.6 jam mcg / ml. Nilai rata-rata jumlah pelepasan dan isipadu pengedaran pada keadaan stabil adalah 21 1 / h / m2 dan 113 L. Perubahan antara individu dalam pelepasan total adalah sekitar 50%. Docetaxel lebih daripada 95% terikat dengan protein plasma.
Satu kajian dengan 14C-docetaxel dilakukan pada tiga pesakit barah. Docetaxel dihilangkan pada air kencing dan najis oleh oksidasi sitokrom P 450 yang diantara kumpulan tertbutyl ester; dalam masa tujuh hari, kira-kira 6% dan 75% radioaktif yang diberikan masing-masing dikeluarkan dalam air kencing dan najis. Kira-kira 80% radioaktiviti yang terdapat pada najis diekskresikan dalam 48 jam pertama sebagai satu metabolit utama dan tiga metabolit kecil yang tidak aktif dan sejumlah kecil ubat induk.
Kajian farmakokinetik populasi dilakukan pada 577 pesakit. Parameter farmakokinetik yang dikira oleh model sangat dekat dengan yang diperhatikan dalam kajian fasa I. Farmakokinetik docetaxel tidak diubah mengikut usia atau jantina pesakit. Dalam sebilangan kecil pesakit (n = 23) dengan hasil biokimia. Menunjukkan hepatik sederhana disfungsi (ALAT, ASAT 3 1.5 kali had atas normal, berkaitan dengan alkali fosfatase 3 2.5 had atas normal), pelepasan total menurun secara purata sebanyak 27% (lihat bahagian 4.2). Pelepasan docetaxel tidak terjejas pada pesakit dengan ringan atau sederhana penahan cecair Tidak ada data yang tersedia pada pesakit dengan penahan cecair yang teruk.
Apabila digunakan dalam kombinasi, docetaxel tidak mempengaruhi pelepasan doxorubicin dan tahap plasma doxorubicinol (metabolit doxorubicin). Farmakokinetik docetaxel, doxorubicin dan cyclophosphamide tidak terjejas oleh pemberian bersama.
Kajian Tahap I yang menilai kesan capecitabine pada farmakokinetik docetaxel dan sebaliknya menunjukkan bahawa tidak ada kesan capecitabine pada farmakokinetik docetaxel (Cmax dan AUC) dan bahawa tidak ada kesan docetaxel pada farmakokinetik metabolit. relevan dengan capecitabine, 5 "-DFUR.
Pelepasan docetaxel dalam terapi kombinasi dengan cisplatin adalah serupa dengan yang diamati semasa monoterapi. Profil farmakokinetik cisplatin diberikan sejurus selepas infus docetaxel serupa dengan yang diamati dengan cisplatin sahaja.
Gabungan pemberian docetaxel, cisplatin dan 5-fluorouracil pada 12 pesakit dengan tumor pepejal tidak mempunyai pengaruh terhadap farmakokinetik setiap produk ubat.
Kesan prednisone pada farmakokinetik docetaxel diberikan dengan premedikasi standard dengan dexamethasone dikaji pada 42 pesakit. Tiada kesan prednisone pada farmakokinetik docetaxel.
05.3 Data keselamatan praklinikal
Potensi karsinogenik docetaxel belum dikaji.
Docetaxel terbukti mutagenik dalam ujian ini secara in vitro penyimpangan kromosom dalam sel CHO-K1 e dalam vivo dalam ujian mikronukleus tikus. Walau bagaimanapun, docetaxel tidak mutagenik dalam ujian Ames atau ujian mutasi gen CHO / HGPRT. Hasil ini selaras dengan aktiviti farmakologi docetaxel.
Kesan yang tidak diingini pada organ kelamin lelaki, yang diperhatikan dalam kajian ketoksikan pada tikus, menunjukkan bahawa docetaxel boleh merosakkan kesuburan lelaki.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Botol pekat:
polysorbate 80, asid sitrik.
Botol pelarut:
95% etanol, air untuk suntikan.
06.2 Ketidaksesuaian
Produk ubat tidak boleh dicampurkan dengan produk lain kecuali yang disebutkan dalam bahagian 6.6.
06.3 Tempoh sah
2 tahun.
Larutan pra-campuran: larutan pra-dicairkan mengandungi 10 mg / ml docetaxel dan mesti digunakan sejurus selepas penyediaan, walaupun kestabilan kimia-fizikal larutan ini telah ditunjukkan selama 8 jam jika disimpan di antara + 2 ° C dan +8 ° C atau pada suhu bilik (di bawah 25 ° C).
Penyelesaian untuk infus: Penyelesaian untuk infus, disimpan pada suhu bilik (di bawah 25 ° C), harus digunakan dalam 4 jam.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Jangan simpan di atas 25 ° C atau di bawah 2 ° C.
Simpan dalam bungkusan asal untuk menjauhkannya dari cahaya.
Untuk keadaan penyimpanan produk ubat yang dicairkan, lihat bahagian 6.3.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
Setiap lepuh mengandungi:
satu botol pekat satu dos dan satu botol pelarut dos tunggal.
Vial TAXOTERE 20 mg / 0.5 ml pekat untuk penyelesaian untuk infus:
7 ml botol kaca bening Jenis I dengan penutup flip off hijau.
Botol mengandungi larutan docetaxel dalam 0,5 ml polysorbate 80 dan kepekatan 40 mg / ml (isian isian: 24,4 mg / 0,61 ml). Isi padu pengisian ini dibuat semasa pengembangan TAXOTERE untuk mengimbangi kehilangan cecair semasa penyediaan larutan yang telah dilarutkan kerana berbuih, lekatan pada dinding botol dan 'ruang mati'. Pengisian berlebihan memastikan bahawa selepas pencairan dengan seluruh kandungan botol pelarut yang dilampirkan dengan TAXOTERE isipadu larutan minimum yang dapat diekstraksi adalah 2 ml, mengandung 10 mg / ml docetaxel yang sesuai dengan kandungan yang dinyatakan pada label 20 mg / 0,5 ml setiap botol.
Botol pelarut:
Botol kaca jernih jenis I 7 ml dengan penutup flip-off jernih tanpa warna.
Botol pelarut mengandungi 1.5 ml larutan 13% (b / b) larutan etanol 95% dalam air untuk suntikan (isian isi: 1.98 ml). Menambah keseluruhan kandungan botol pelarut ke dalam TAXOTERE 20 mg / 0.5 ml, pekatan untuk larutan untuk infusi memastikan bahawa larutan pramampuran diperoleh dengan kepekatan 10 mg / ml docetaxel.
06.6 Arahan penggunaan dan pengendalian
TAXOTERE adalah ubat antineoplastik dan, seperti produk berpotensi toksik lain, perlu berhati-hati dalam menangani dan menyediakan penyelesaian. Digunakan penggunaan sarung tangan. Sekiranya TAXOTERE dalam bentuk pekat, pra-dicairkan atau larutan untuk infusi harus bersentuhan dengan kulit, basuh segera dan bersih dengan sabun dan air. hendaklah bersentuhan dengan selaput lendir, segera basuh dengan air.
Persediaan untuk pentadbiran intravena
a) Penyediaan larutan siap pakai TAXOTERE (10 mg docetaxel / ml)
Sekiranya botol disimpan di dalam peti sejuk, biarkan bilangan kotak TAXOTERE yang diperlukan pada suhu bilik (di bawah 25 ° C) selama 5 minit.
Dengan menggunakan jarum suntik bertahap dengan jarum, tarik keseluruhan kandungan botol pelarut untuk TAXOTERE dengan membalikkan botol tersebut sebahagiannya.
Suntikkan keseluruhan kandungan jarum suntik ke dalam botol TAXOTERE yang sesuai.
Keluarkan jarum suntik dan jarum dan campurkan larutan secara manual dengan membalikkan berulang kali selama 45 saat. Jangan goncang.
Biarkan botol larutan yang telah dilarutkan selama 5 minit pada suhu bilik (di bawah 25 ° C) dan kemudian periksa bahawa larutan itu jelas dan homogen. (Pembuahan adalah normal walaupun selepas 5 minit kerana kandungan polysorbate 80 dalam formulasi).
Larutan yang telah dicairkan mengandungi 10 mg / ml docetaxel dan mesti digunakan sejurus selepas penyediaan, walaupun kestabilan kimia-fizikal larutan ini telah ditunjukkan selama 8 jam jika disimpan antara + 2 ° C hingga + 8 ° C atau pada suhu bilik (di bawah 25 ° C).
b) Penyediaan penyelesaian untuk infusi
Beberapa botol larutan yang telah dicairkan mungkin diperlukan untuk mendapatkan dos pesakit yang diperlukan. Berdasarkan dos yang diperlukan untuk pesakit yang dinyatakan dalam mg, tarik secara isipadu jumlah larutan larutan yang sesuai yang mengandung 10 mg / ml docetaxel dari sejumlah botol larutan predilutasi yang sesuai menggunakan jarum suntikan bertahap. Sebagai contoh, untuk dos docetaxel 140 mg, 14 ml larutan docetaxel yang telah diprutilasi harus ditarik. Suntikan isipadu larutan yang diencerkan ke dalam beg atau botol 250 ml yang mengandungi larutan glukosa 5% atau larutan untuk infus dengan 9 mg / ml natrium klorida (0,9%).
Sekiranya dos docetaxel lebih besar daripada 200 mg diperlukan, gunakan isipadu larutan infus yang lebih besar sehingga kepekatan docetaxel tidak melebihi 0.74 mg / ml. Campurkan beg atau botol secara manual dengan gerakan memutar.
Penyelesaian TAXOTERE untuk infusi harus digunakan dalam 4 jam dan harus diberikan sebagai infus 1 jam, secara aseptik, pada suhu bilik (di bawah 25 ° C) dan dalam keadaan cahaya normal.
Seperti semua produk untuk penggunaan parenteral, larutan yang telah diencerkan dan larutan perfusi dari TAXOTERE mesti diperiksa secara visual sebelum digunakan, larutan yang mengandung endapan mesti dibuang.
Produk dan sisa yang tidak digunakan yang berasal dari ubat ini mesti dibuang sesuai dengan kehendak undang-undang tempatan.
07.0 PEMEGANG KEBENARAN PEMASARAN
Aventis Pharma S.A., 20 Avenue Raymond Aron, 92165 Antony Cedex, Perancis
08.0 NOMBOR KEBENARAN PEMASARAN
EU / 1/95/002/001
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Tarikh kebenaran pertama: 27 November 1995
Tarikh pembaharuan terakhir: 27 November 2005.









-propriet-nutrizionali.jpg)