Bahan aktif: Etoricoxib
EXINEF 30 mg tablet bersalut filem
EXINEF 60 mg tablet bersalut filem
EXINEF 90 mg tablet bersalut filem
EXINEF 120 mg tablet bersalut filem
Mengapa Exinef digunakan? Untuk apa itu?
- EXINEF tergolong dalam kumpulan ubat yang dipanggil inhibitor COX-2 terpilih. Ini milik keluarga ubat-ubatan yang dikenali sebagai ubat anti-radang bukan steroid (NSAID).
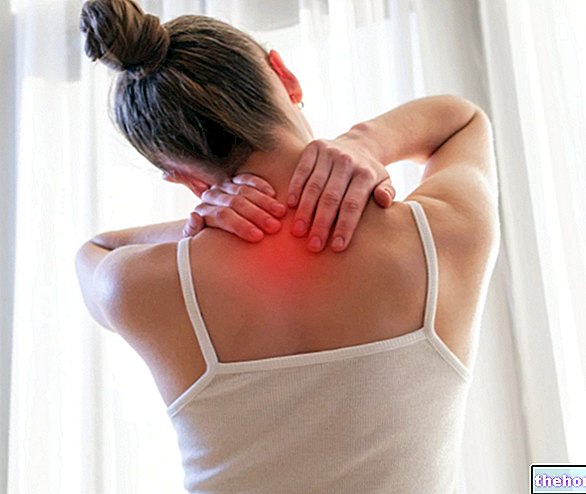
- EXINEF membantu mengurangkan kesakitan dan pembengkakan (keradangan) pada sendi dan otot orang dengan osteoartritis, rheumatoid arthritis, ankylosing spondylitis dan gout.
- EXINEF juga digunakan untuk rawatan jangka pendek kesakitan sederhana selepas pembedahan pergigian.
Apa itu osteoartritis (OA)?
Osteoarthritis adalah penyakit sendi. Ia disebabkan oleh kemerosotan tulang rawan yang progresif yang menutupi hujung tulang. Ini menyebabkan pembengkakan (keradangan), sakit, kelembutan, kekakuan dan kecacatan.
Apa itu artritis reumatoid?
Rheumatoid arthritis adalah penyakit sendi radang jangka panjang. Ia menyebabkan rasa sakit, kekakuan, bengkak, dan kehilangan pergerakan secara progresif pada sendi yang terjejas. Ia juga boleh menyebabkan keradangan di bahagian lain badan.
Apa itu gout?
Gout adalah penyakit dengan serangan radang dan kemerahan pada sendi yang tiba-tiba dan berulang. Ia disebabkan oleh pemendapan kristal mineral di sendi.
Apakah spondylitis ankylosing?
Ankylosing spondylitis adalah penyakit radang tulang belakang dan sendi besar.
Kontraindikasi Apabila Exinef tidak boleh digunakan
Jangan mengambil EXINEF:
- jika anda alah (hipersensitif) terhadap etoricoxib atau mana-mana bahan lain dari EXINEF (lihat Maklumat Lanjut
- jika anda alah kepada ubat anti-radang bukan steroid (NSAID), termasuk perencat aspirin dan COX-2 (lihat Kemungkinan kesan sampingan)
- jika anda mempunyai ulser perut aktif atau pendarahan perut atau usus aktif
- jika anda mempunyai penyakit hati yang teruk
- jika anda menghidap penyakit buah pinggang yang teruk
- jika anda hamil atau ada kemungkinan anda hamil, atau jika anda menyusu (lihat "Kehamilan dan penyusuan")
- sekiranya anda berumur di bawah 16 tahun
- jika anda mempunyai penyakit radang usus seperti penyakit Crohn, kolitis ulseratif, atau kolitis
- jika doktor anda telah mendiagnosis anda dengan masalah jantung seperti kegagalan jantung (sederhana atau teruk), angina (sakit dada); atau jika anda pernah mengalami serangan jantung; o sekiranya anda telah menjalani pembedahan pintasan arteri koronari; jika anda mempunyai "penyakit arteri perifer (pengurangan peredaran darah di kaki dan kaki kerana saluran darah yang menyempit atau tersumbat) atau jika anda pernah mengalami jenis strok (termasuk stroke mini, serangan iskemia sementara atau TIA)." etoricoxib boleh meningkat sedikit risiko serangan jantung dan strok; untuk alasan ini tidak boleh digunakan pada orang yang sudah mengalami masalah jantung atau strok
- jika anda mempunyai tekanan darah tinggi yang tidak dikendalikan oleh rawatan (tanyakan kepada doktor atau ahli farmasi anda jika anda tidak pasti sama ada tekanan darah anda dikawal dengan secukupnya).
Sekiranya anda berpendapat bahawa semua ini berlaku untuk anda, jangan ambil tablet ini sehingga anda berjumpa doktor.
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Exinef
Bercakap dengan doktor atau ahli farmasi anda sebelum mengambil EXINEF jika:
- Mempunyai sejarah pendarahan perut atau bisul.
- Anda mengalami dehidrasi, misalnya kerana episod muntah atau cirit-birit yang berpanjangan.
- Anda mengalami pembengkakan kerana pengekalan cecair.
- Mempunyai sejarah kegagalan jantung, atau bentuk penyakit jantung yang lain.
- Mempunyai sejarah tekanan darah tinggi. Pada sesetengah orang, EXINEF, terutama dalam dos tinggi, dapat meningkatkan tekanan darah, dan doktor anda akan memeriksa tekanan darah anda secara berkala.
- Mempunyai sejarah penyakit hati atau buah pinggang.
- Dia sedang dirawat karena jangkitan. EXINEF dapat menyembunyikan atau menyembunyikan demam, yang merupakan tanda jangkitan.
- Dia adalah wanita yang sedang berusaha untuk hamil.
- Dia adalah orang tua (berumur lebih dari 65 tahun).
- Anda menghidap diabetes, kolesterol tinggi atau kebiasaan merokok. Ini adalah keadaan yang boleh meningkatkan risiko penyakit jantung anda.
Sekiranya anda tidak pasti mengenai apa-apa keadaan yang baru disebutkan, berbincanglah dengan doktor anda sebelum mengambil EXINEF untuk mengetahui apakah ubat tersebut sesuai untuk anda.
EXINEF mempunyai khasiat yang sama pada pesakit yang lebih muda dan lebih tua. Sekiranya anda berumur (lebih dari 65 tahun), doktor anda akan memantau anda dengan betul. Tidak perlu penyesuaian dos untuk pesakit tua.
Kanak-kanak dan remaja
Jangan berikan ubat ini kepada kanak-kanak dan remaja di bawah 16 tahun.
Interaksi Ubat atau makanan mana yang boleh mengubah kesan Exinef
Beritahu doktor atau ahli farmasi anda jika anda mengambil, baru-baru ini mengambil atau mungkin mengambil ubat lain, termasuk yang ada tanpa preskripsi doktor.
Khususnya, jika anda mengambil salah satu ubat berikut, doktor anda mungkin meminta anda untuk memeriksa sama ada ubat-ubatan ini berfungsi dengan baik setelah anda mula mengambil EXINEF:
- pengencer darah (antikoagulan), seperti warfarin
- rifampicin (antibiotik)
- methotrexate (ubat yang digunakan untuk menekan sistem kekebalan tubuh dan sering digunakan dalam rawatan artritis reumatoid)
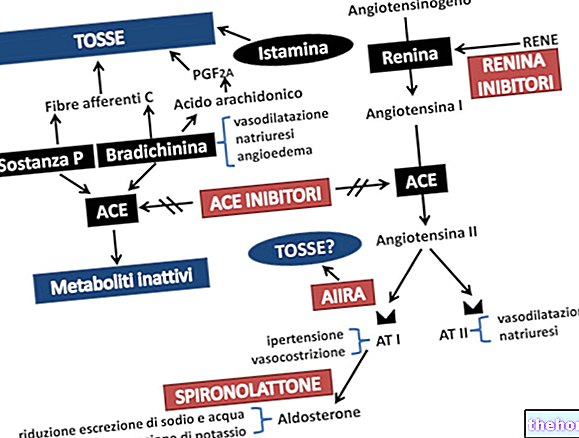
- ubat-ubatan yang digunakan untuk tekanan darah tinggi dan kegagalan jantung yang disebut ACE inhibitor dan penghambat reseptor angiotensin, seperti enalapril dan ramipril, dan losartan dan valsartan
- litium (ubat yang digunakan untuk beberapa jenis kemurungan)
- diuretik
- siklosporin atau tacrolimus (ubat yang digunakan untuk menekan sistem imun)
- digoxin (ubat untuk merawat kegagalan jantung dan irama jantung yang tidak teratur)
- minoxidil (ubat untuk merawat tekanan darah tinggi)
- tablet salbutamol atau larutan oral (ubat untuk merawat asma)
- kontraseptif oral
- terapi penggantian hormon
- aspirin, risiko ulser perut lebih tinggi jika anda mengambil EXINEF dengan aspirin.
EXINEF boleh diambil dengan dos aspirin yang rendah. Sekiranya anda dirawat dengan aspirin dosis rendah untuk mencegah serangan jantung atau strok, anda tidak boleh berhenti mengambil aspirin tanpa berunding dengan doktor anda.
Anda tidak boleh mengambil aspirin atau ubat anti-radang dalam dos yang tinggi semasa mengambil EXINEF.
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Tablet EXINEF tidak boleh diambil semasa mengandung. Sekiranya anda hamil atau disyaki mengandung, atau jika anda fikir anda mungkin hamil, jangan ambil tablet. Sekiranya anda hamil, hentikan pengambilan tablet dan berjumpa doktor.
Sekiranya anda tidak pasti atau jika anda memerlukan lebih banyak maklumat mengenai perkara ini, berjumpa dengan doktor anda. Tidak diketahui sama ada EXINEF diekskresikan dalam susu manusia. Sekiranya anda menyusu, atau fikir anda akan menyusui, hubungi doktor anda sebelum mengambil EXINEF. Sekiranya anda menggunakan EXINEF, anda tidak boleh menyusu.
KELUAR dengan makanan dan minuman
Permulaan kesan EXINEF mungkin lebih cepat apabila diambil tanpa makanan.
Memandu atau menggunakan mesin
Beberapa pesakit yang mengambil EXINEF telah melaporkan pening dan mengantuk.
Jangan memandu jika anda merasa pening atau mengantuk.
Jangan gunakan alat atau mesin jika anda merasa pening atau mengantuk.
EXINEF mengandungi laktosa
Sekiranya anda diberitahu oleh doktor bahawa anda tidak boleh bertolak ansur dengan gula, hubungi doktor anda sebelum mengambil ubat ini
Dos, Kaedah dan Masa Pentadbiran Cara menggunakan Exinef: Posologi
Selalu minum ubat ini tepat seperti yang diberitahu oleh doktor anda. Sekiranya anda ragu-ragu, berjumpa dengan doktor atau ahli farmasi anda.
Tablet EXINEF tidak boleh diambil oleh kanak-kanak atau remaja di bawah 16 tahun.
Ambil tablet EXINEF sekali sehari melalui mulut. EXINEF boleh diambil dengan atau tanpa makanan.
Jangan mengambil lebih daripada dos yang disyorkan untuk rawatan penyakit anda. Doktor anda akan menilai rawatan anda secara berkala. Anda mesti menggunakan dos kawalan kesakitan yang paling rendah dan anda tidak mengambil EXINEF lebih lama daripada yang diperlukan. Ini kerana risiko serangan jantung dan strok dapat meningkat setelah rawatan berpanjangan, terutama dengan dos yang tinggi.
Arthrosis
Dos yang disyorkan adalah 30 mg sekali sehari, yang dapat ditingkatkan hingga maksimum 60 mg sekali sehari jika perlu.
Artritis reumatoid
Dos yang disyorkan adalah 90 mg sekali sehari.
Spondylitis ankylosing
Dos yang disyorkan adalah 90 mg sekali sehari. Keadaan kesakitan akut Etoricoxib hanya boleh digunakan untuk tempoh sakit akut.
Gout
Dos yang disyorkan adalah 120 mg sekali sehari, yang hanya boleh digunakan untuk tempoh sakit akut, sehingga maksimum 8 hari rawatan.
Kesakitan selepas operasi dari pembedahan pergigian
Dos yang disyorkan adalah 90 mg sekali sehari, terhad untuk maksimum 3 hari rawatan.
Orang yang mempunyai masalah hati
- Sekiranya anda mempunyai penyakit hati yang ringan, anda tidak boleh mengambil lebih daripada 60 mg sehari.
- Sekiranya anda mempunyai penyakit hati yang sederhana, anda tidak boleh mengambil lebih daripada 30 mg sehari.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Exinef
Sekiranya anda mengambil LEBIH CEPAT daripada yang sepatutnya
Anda tidak boleh mengambil lebih banyak tablet daripada yang disyorkan oleh doktor anda. Sekiranya anda mengambil terlalu banyak tablet EXINEF, anda harus segera berjumpa doktor.
Sekiranya anda terlupa mengambil EXINEF
Penting untuk mematuhi dos EXINEF yang ditunjukkan oleh doktor anda. Sekiranya anda lupa dos, mulakan semula jadual dos biasa anda pada hari berikutnya. Jangan mengambil dos berganda untuk menggantikan tablet yang dilupakan.
Sekiranya anda mempunyai pertanyaan lebih lanjut mengenai penggunaan ubat ini, tanyakan kepada doktor atau ahli farmasi anda.
Kesan Sampingan Apakah kesan sampingan Exinef
Seperti semua ubat, EXINEF boleh menyebabkan kesan sampingan, tetapi tidak berlaku pada semua pesakit.
Sekiranya ada gejala berikut, anda harus berhenti mengambil EXINEF dan segera hubungi doktor anda:
- sesak nafas, sakit dada, atau pembengkakan pergelangan kaki yang berkembang atau mula bertambah teruk
- menguning kulit dan mata (penyakit kuning) - ini adalah gejala masalah hati
- sakit perut atau najis yang teruk atau berterusan yang bertukar menjadi hitam
- reaksi alahan yang mungkin merangkumi masalah kulit seperti bisul atau lepuh, atau pembengkakan muka, bibir, lidah, atau tekak yang boleh menyukarkan pernafasan.
Kekerapan kemungkinan kesan sampingan yang disenaraikan di bawah ditentukan berdasarkan konvensyen berikut:
Sangat biasa (mempengaruhi lebih daripada 1 dari 10 pesakit)
Biasa (mempengaruhi 1 hingga 10 pengguna dalam 100)
Tidak biasa (mempengaruhi 1 hingga 10 pengguna dalam 1,000)
Jarang (mempengaruhi 1 hingga 10 pengguna dalam 10,000)
Sangat jarang berlaku (mempengaruhi kurang daripada 1 pengguna dalam 10,000)
Kesan sampingan berikut mungkin berlaku semasa rawatan dengan EXINEF:
Sangat biasa:
- sakit perut
Biasa:
- alveolitis (keradangan dan kesakitan selepas "pencabutan gigi)
- bengkak kaki dan / atau kaki kerana penahan cecair (edema)
- pening, sakit kepala
- berdebar-debar (degupan jantung cepat atau tidak teratur), irama jantung tidak teratur (aritmia)
- peningkatan tekanan darah
- berdehit atau sesak nafas (bronkospasme)
- sembelit, kembung perut (berlebihan gas), gastritis (keradangan permukaan dalam perut), pedih ulu hati, cirit-birit, senak (dispepsia) / ketidakselesaan perut, mual, muntah (muntah), radang esofagus, ulser mulut
- perubahan dalam beberapa ujian darah yang berkaitan dengan fungsi hati
- lebam
- kelemahan dan keletihan, penyakit seperti selesema
Tidak biasa:
- gastroenteritis (keradangan saluran gastrointestinal yang melibatkan perut dan usus kecil), jangkitan pernafasan atas, jangkitan saluran kencing
- penurunan bilangan sel darah merah, penurunan jumlah sel darah putih, penurunan platelet
- hipersensitiviti (reaksi alahan termasuk gatal-gatal yang mungkin cukup teruk sehingga memerlukan rawatan perubatan segera)
- kenaikan atau penurunan selera makan, kenaikan berat badan
- kegelisahan, kemurungan, penurunan ketajaman mental, persepsi visual, sensitif atau pendengaran yang tidak disebabkan oleh rangsangan sebenar (halusinasi)
- perubahan rasa, sukar tidur, kesemutan atau mati rasa, mengantuk
- penglihatan kabur, kerengsaan dan kemerahan mata
- berdering di telinga, vertigo (perasaan pening berterusan)
- irama jantung yang tidak normal (fibrilasi atrium), degupan jantung yang cepat, kegagalan jantung, sesak, tekanan atau rasa berat di dada (angina pectoris), serangan jantung
- flushing, stroke, mini-stroke (serangan iskemia sementara), peningkatan tekanan darah yang teruk, radang saluran darah
- batuk, sesak nafas, mimisan
- kembung perut atau usus, perubahan tabiat usus, mulut kering, ulser perut, keradangan pada permukaan dalam perut yang boleh menjadi teruk dan boleh menyebabkan pendarahan, sindrom iritasi usus, radang pankreas
- bengkak muka, ruam kulit atau kulit gatal, kemerahan kulit
- kekejangan otot / kekejangan, sakit otot / kekejangan
- kadar kalium yang tinggi dalam darah, perubahan dalam beberapa ujian darah atau air kencing yang berkaitan dengan fungsi buah pinggang, masalah buah pinggang yang teruk
- sakit dada
Jarang:
- angioedema (reaksi alergi dengan pembengkakan muka, bibir, lidah dan / atau tekak yang boleh menyebabkan kesukaran bernafas dan menelan, yang mungkin cukup teruk sehingga memerlukan rawatan perubatan segera) / reaksi anafilaksis / anafilaktoid termasuk kejutan (reaksi alergi yang teruk yang memerlukan rawatan perubatan segera)
- kekeliruan, kegelisahan
- masalah hati (hepatitis)
- tahap natrium rendah dalam darah
- kegagalan hati, menguning kulit dan / atau mata (penyakit kuning)
- reaksi kulit yang teruk
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini.
Tamat Tempoh dan Pengekalan
Jauhkan ubat ini dari pandangan dan jangkauan kanak-kanak.
Jangan mengambil EXINEF selepas tarikh luput yang tertera pada bungkusan. Tarikh luput merujuk pada hari terakhir bulan yang dinyatakan.
Botol: Pastikan bekas ditutup rapat untuk melindungi ubat daripada kelembapan.
Lepuh: Simpan dalam bungkusan asli untuk melindungi ubat daripada kelembapan.
Jangan buang ubat melalui air buangan atau sampah rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Apa yang mengandungi EXINEF
- Bahan aktif adalah etoricoxib. Setiap tablet bersalut filem mengandungi 30, 60, 90 atau 120 mg etoricoxib.
- Bahan-bahan lain adalah:
Di dalam tablet: kalsium fosfat dibasik anhidrat, natrium croscarmellose, magnesium stearate, selulosa mikrokristal.
Lapisan tablet: carnauba wax, lactose monohydrate, hypromellose, titanium dioxide (E171), triacetin. Tablet 30, 60 dan 120 mg juga mengandungi oksida besi kuning (warna E172) dan indigo carmine (warna E132).
Seperti apa EXINEF dan bungkusannya
Tablet EXINEF boleh didapati dalam empat formulasi:
Tablet biconvex 30 mg, berbentuk epal, biru-hijau, dengan huruf "101" di satu sisi dan "ACX 30" di sisi lain
60 mg, biconvex, berbentuk epal, tablet hijau gelap, dengan huruf "200" di satu sisi dan polos di sisi lain;
90 mg, biconvex, berbentuk epal, tablet putih yang bertuliskan "202" di satu sisi dan polos di sisi lain;
120 mg, biconvex, berbentuk epal, tablet hijau muda, dengan huruf "204" di satu sisi dan polos di sisi lain.
Pembungkusan:
30 mg:
Pek 2, 7, 14, 20, 28, 49 tablet atau pelbagai pek 98 (2 bungkus 49) tablet dalam lepuh.
60, 90 dan 120 mg:
Pek 2, 5, 7, 10, 14, 20, 28, 30, 50, 84, 100 tablet atau pelbagai pek 98 (2 pek 49) tablet dalam lepuh; atau 30 dan 90 tablet dalam botol, dengan bekas pengering. Bahan pengering (satu atau dua bekas) di dalam botol, digunakan untuk menjaga agar tablet tetap kering, tidak boleh ditelan.
Tidak semua saiz pek boleh dipasarkan.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
KECUALI
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Setiap tablet bersalut filem mengandungi 30, 60, 90 atau 120 mg etoricoxib.
Eksipien dengan kesan yang diketahui:
30 mg: laktosa 1.3 mg
60 mg: laktosa 2.7 mg
90 mg: laktosa 4.0 mg
120 mg: laktosa 5.3 mg
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI
Tablet bersalut filem (tablet).
Tablet 30 mg: Hijau-biru, berbentuk epal, tablet biconvex, dengan huruf "101" di satu sisi dan "ACX 30" di sisi lain.
Tablet 60 mg: hijau gelap, berbentuk epal, tablet biconvex, bertuliskan "200" di satu sisi dan polos di sisi lain.
Tablet 90 mg: Tablet putih, berbentuk epal, biconvex yang bertuliskan "202" di satu sisi dan polos di sisi lain.
Tablet 120 mg: tablet biconvex berbentuk epal, hijau muda, dengan huruf "204" di satu sisi dan polos di sisi lain.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Untuk rawatan simptomatik osteoarthritis (OA), rheumatoid arthritis (RA), ankylosing spondylitis dan kesakitan dan tanda-tanda keradangan yang berkaitan dengan arthritis gout akut.
Untuk rawatan jangka pendek kesakitan sederhana yang berkaitan dengan pembedahan pergigian.
Keputusan untuk menetapkan perencat COX-2 selektif harus berdasarkan pada penilaian risiko keseluruhan pesakit (lihat bahagian 4.3, 4.4).
04.2 Posologi dan kaedah pentadbiran
Dos
Oleh kerana risiko kardiovaskular etoricoxib boleh meningkat dengan dos dan tempoh pendedahan, tempoh rawatan harus sesingkat mungkin dan dos harian efektif terendah harus digunakan. Keperluan rawatan untuk melegakan simptomatik dan tindak balas terhadap terapi harus dinilai semula secara berkala, terutama pada pesakit dengan osteoartritis (lihat bahagian 4.3, 4.4, 4.8 dan 5.1).
Osteoartritis
Dos yang disyorkan ialah 30 mg sekali sehari. Pada sesetengah pesakit dengan gejala yang tidak mencukupi, peningkatan dos hingga 60 mg sekali sehari dapat meningkatkan keberkesanannya. Sekiranya tidak ada faedah terapeutik yang meningkat, alternatif terapi lain harus dipertimbangkan.
Artritis reumatoid
Dos yang disyorkan adalah 90 mg sekali sehari.
Spondylitis ankylosing
Dos yang disyorkan adalah 90 mg sekali sehari.
Untuk keadaan sakit akut, etoricoxib hanya boleh digunakan semasa fasa gejala akut.
Artritis gout akut
Dos yang disyorkan ialah 120 mg sekali sehari. Dalam ujian klinikal artritis gouty akut, etoricoxib diberikan selama 8 hari.
Kesakitan selepas operasi dari pembedahan gigi
Dos yang disyorkan adalah 90 mg sekali sehari, terhad maksimum 3 hari. Beberapa pesakit mungkin memerlukan "analgesia pasca operasi."
Dos yang lebih tinggi daripada yang disyorkan untuk setiap petunjuk tidak menunjukkan keberkesanan yang lebih besar atau belum dipelajari. Akibatnya:
Dos untuk OA tidak boleh melebihi 60 mg / hari.
Dos untuk RA dan ankylosing spondylitis tidak boleh melebihi 90 mg / hari.
Dos untuk artritis gout akut tidak boleh melebihi 120 mg / hari, terhad kepada maksimum 8 hari rawatan.
Dos untuk kesakitan pasca operasi akut dari pembedahan pergigian tidak boleh melebihi 90 mg / hari, terhad maksimum 3 hari.
Populasi khas
Warga emas
Tiada penyesuaian dos yang diperlukan pada orang tua. Seperti ubat lain, berhati-hati harus dilakukan pada pesakit tua (lihat bahagian 4.4).
Kekurangan hepatik
Tanpa mengira petunjuk, dos 60 mg sekali sehari tidak boleh dilebihi pada pesakit dengan disfungsi hepatik ringan (skor Child-Pugh 5-6). Pada pesakit dengan disfungsi hepatik sederhana (skor Child-Pugh 7-9), tanpa mengira petunjuk, dos 30 mg sekali sehari tidak boleh dilebihi.
Pengalaman klinikal sangat terhad pada pesakit dengan disfungsi hepatik sederhana dan berhati-hati harus dilakukan. Tidak ada pengalaman klinikal pada pesakit dengan disfungsi hepatik yang teruk (skor Child-Pugh ≥10); oleh itu penggunaan ubat ini dikontraindikasikan. Pada pesakit ini (lihat bahagian 4.3, 4.4 dan 5.2).
Kegagalan buah pinggang
Tidak diperlukan penyesuaian dos untuk pesakit dengan izin kreatinin ≥30 ml / min (lihat bahagian 5.2). Penggunaan etoricoxib pada pesakit dengan pelepasan kreatinin
Pesakit kanak-kanak
Etoricoxib dikontraindikasikan pada kanak-kanak dan remaja di bawah usia 16 tahun (lihat bahagian 4.3).
Kaedah pentadbiran
EXINEF diberikan secara oral dan boleh diambil dengan atau tanpa makanan. Permulaan kesan produk ubat dapat dijangkakan ketika EXINEF diberikan di antara waktu makan. Perkara ini harus diambil kira sekiranya diperlukan penolakan gejala yang cepat.
04.3 Kontraindikasi
Hipersensitiviti terhadap bahan aktif atau sebarang bahan tambahan produk ini yang disenaraikan dalam bahagian 6.1.
Ulser peptik aktif atau pendarahan gastrousus (GI) aktif.
Pesakit yang mengalami bronkospasme, rhinitis akut, polip hidung, edema angioneurotik, urtikaria atau reaksi jenis alahan setelah mengambil asid asetilsalisilat atau NSAID termasuk perencat COX-2 (cyclooxygenase-2).
Kehamilan dan penyusuan (lihat bahagian 4.6 dan 5.3).
Disfungsi hepatik yang teruk (albumin serum
Anggaran pelepasan kreatinin buah pinggang
Kanak-kanak dan remaja di bawah umur 16 tahun.
Keradangan kronik usus.
Kegagalan jantung kongestif (NYHA II-IV).
Pesakit hipertensi yang tekanan darahnya berterusan melebihi 140/90 mmHg dan tidak dikawal dengan secukupnya.
Penyakit jantung iskemia, penyakit arteri periferal dan / atau penyakit vaskular serebrum.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
Kesan gastrousus
Komplikasi gastrointestinal atas [perforasi, bisul atau pendarahan (SUP)] telah berlaku pada pesakit yang dirawat dengan etoricoxib, beberapa di antaranya membawa maut.
Berhati-hati apabila merawat pesakit yang paling berisiko mengalami komplikasi gastrointestinal dengan NSAID: orang tua, pesakit yang mengambil NSAID lain atau asid acetylsalicylic bersamaan, atau pesakit dengan riwayat gangguan gastrointestinal, seperti bisul dan pendarahan saluran gastrointestinal.
Apabila etoricoxib diambil bersama-sama dengan asid acetylsalicylic (walaupun pada dos rendah), terdapat peningkatan risiko kesan buruk gastrointestinal (ulser gastrousus atau komplikasi gastrointestinal lain). (lihat bahagian 5.1).
Kesan kardiovaskular
Kajian klinikal menunjukkan bahawa kelas ubat penghambat COX-2 selektif mungkin dikaitkan dengan risiko kejadian trombotik (terutamanya infark dan strok miokard MI), berbanding dengan plasebo dan beberapa NSAID. Oleh kerana risiko kardiovaskular etoricoxib boleh meningkat dengan dos dan tempoh pendedahan, tempoh rawatan harus sesingkat mungkin dan dos harian efektif terendah harus digunakan. Keperluan rawatan dan tindak balas terhadap terapi harus dinilai semula secara berkala, terutama pada pesakit dengan osteoartritis (lihat bahagian 4.2, 4.3, 4.8 dan 5.1).
Pesakit dengan faktor risiko yang signifikan untuk kejadian kardiovaskular (mis. Hipertensi, hiperlipidemia, diabetes mellitus, kebiasaan merokok) hanya boleh dirawat dengan etoricoxib setelah dipertimbangkan dengan teliti (lihat bahagian 5.1).
Inhibitor COX-2 selektif tidak menggantikan asid asetilsalisilat dalam profilaksis penyakit kardiovaskular tromboemboli kerana tidak mempunyai kesan antiplatelet. Oleh itu, terapi antiplatelet tidak boleh dihentikan (lihat bahagian 4.5 dan 5.1).
Kesan buah pinggang
Prostaglandin ginjal dapat memainkan peranan kompensasi dalam menjaga perfusi buah pinggang. Oleh itu, dalam keadaan perfusi ginjal yang terganggu, pemberian etoricoxib boleh mengakibatkan pengurangan pengeluaran prostaglandin dan, kedua, aliran darah ginjal dan dengan itu mengganggu fungsi ginjal. gangguan, kegagalan jantung dekompensasi atau sirosis. Pemantauan fungsi ginjal harus dipertimbangkan pada pesakit tersebut.
Pengekalan cecair, edema dan hipertensi
Seperti produk perubatan lain yang diketahui menghalang sintesis prostaglandin, pengekalan cairan, edema dan hipertensi telah diperhatikan pada pesakit yang menggunakan etoricoxib. Semua Ubat Anti-Radang Bukan Steroid (NSAID), termasuk etoricoxib, boleh dikaitkan dengan permulaan kegagalan jantung kongestif atau kambuhannya. Untuk maklumat mengenai tindak balas terapi etorikoksib yang berkaitan dengan dos, lihat bahagian 5.1.
Perhatian harus diberikan pada pesakit dengan riwayat kegagalan jantung, disfungsi ventrikel kiri atau hipertensi dan pada pesakit dengan edema yang sudah ada atas sebab lain. Sekiranya terdapat bukti klinikal kemerosotan keadaan pesakit ini, langkah-langkah yang sesuai harus diambil, termasuk penghentian terapi etorikoksib.
Etoricoxib mungkin dikaitkan dengan hipertensi yang lebih teruk dan lebih kerap daripada NSAID lain dan perencat COX-2 selektif, terutamanya pada dos tinggi. Oleh itu, hipertensi harus dikawal sebelum rawatan dengan etoricoxib (lihat bahagian 4.3) dan perhatian khusus harus diberikan kepada pemantauan tekanan darah selama rawatan dengan etoricoxib. Tekanan darah harus dipantau dalam waktu 2 minggu sejak permulaan rawatan. Dan kemudian secara berkala. Sekiranya tekanan darah meningkat dengan ketara, rawatan alternatif harus dipertimbangkan.
Kesan hepatik
Dalam kajian klinikal, peningkatan etanicoxib alanine aminotransferase (ALT) dan / atau aspartate aminotransferase (AST) telah dilaporkan pada kira-kira 1% pesakit yang dirawat dengan etorikoksib 30, 60 dan 90 mg sehari sehingga (satu tahun atau lebih) kali ganda had atas norma).
Pesakit dengan tanda dan / atau gejala disfungsi hati atau dengan ujian fungsi hati yang tidak normal harus dinilai. Sekiranya terdapat tanda-tanda kegagalan hati atau terdapat kelainan berterusan (tiga kali lebih tinggi daripada biasa) dalam ujian fungsi hati, rawatan dengan etoricoxib harus dihentikan.
Langkah berjaga-jaga secara umum
Sekiranya selama rawatan pesakit mengalami kemerosotan fungsi sistem organ yang dijelaskan di atas, langkah-langkah yang sesuai harus diambil dan penghentian terapi etorikoksib harus dipertimbangkan. Pesakit tua dan mereka yang mengalami disfungsi ginjal, hati atau jantung yang dirawat dengan etoricoxib harus disimpan di bawah pemerhatian perubatan yang mencukupi.
Berhati-hati ketika memulakan rawatan dengan etoricoxib pada pesakit yang mengalami dehidrasi. Sebaiknya rehidrasi pesakit sebelum memulakan terapi dengan etoricoxib.
Reaksi kulit yang serius, ada di antaranya yang membawa maut, termasuk dermatitis pengelupasan, sindrom Stevens-Johnson, dan nekrolisis epidermis toksik, jarang sekali dilaporkan dalam pengalaman selepas pemasaran berkaitan dengan penggunaan NSAID dan beberapa perencat COX-2 terpilih (lihat bahagian 4.8). Pesakit nampaknya berisiko lebih tinggi untuk reaksi ini semasa fasa awal terapi, dengan permulaan gejala dalam kebanyakan kes pada bulan pertama rawatan. Reaksi hipersensitiviti serius telah dilaporkan pada pesakit yang dirawat dengan etoricoxib (seperti anafilaksis dan angioedema) (lihat bahagian 4.8). Beberapa perencat COX-2 terpilih telah dikaitkan dengan peningkatan risiko reaksi kulit pada pesakit dengan riwayat alergi ubat. Rawatan dengan etoricoxib harus dihentikan apabila tanda-tanda pertama ruam kulit, lesi mukosa atau yang lain tanda-tanda hipersensitiviti.
Etoricoxib dapat menyembunyikan demam dan tanda-tanda keradangan lain.
Perhatian harus diberikan apabila etoricoxib diberikan bersamaan dengan warfarin atau antikoagulan oral lain (lihat bahagian 4.5).
Penggunaan etoricoxib, seperti ubat lain yang diketahui menghalang sintesis siklooksigenase / prostaglandin, tidak digalakkan pada wanita yang merancang untuk hamil (lihat bahagian 4.6, 5.1 dan 5.3).
Tablet EXINEF mengandungi laktosa. Pesakit dengan masalah keturunan yang jarang berlaku terhadap intoleransi galaktosa, kekurangan Lapp laktase atau penyerapan glukosa-galaktosa tidak boleh mengambil ubat ini.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Interaksi farmakodinamik
Antikoagulan oral: Pada subjek yang stabil pada terapi warfarin kronik, pemberian etoricoxib 120 mg / hari dikaitkan dengan peningkatan kira-kira 13% dalam International Normalized Ratio (INR) masa prothrombin. Oleh itu, INR masa prothrombin pesakit yang menerima antikoagulan oral harus dipantau secara ketat, terutama pada hari-hari pertama, ketika memulakan terapi dengan etoricoxib atau ketika mengubah dos etoricoxib (lihat bahagian 4.4).
Diuretik, perencat ACE dan Angiotensin II-Antagonis (AII-A): NSAID boleh mengurangkan kesan diuretik dan ubat antihipertensi lain. Pada sesetengah pesakit dengan fungsi ginjal yang terganggu (misalnya pesakit yang mengalami dehidrasi atau pesakit tua dengan fungsi ginjal yang terganggu) pemberian bersamaan perencat ACE atau antagonis reseptor angiotensin II dan agen penghambat siklooksigenase boleh menyebabkan untuk kemerosotan fungsi ginjal, termasuk kemungkinan kegagalan buah pinggang akut, yang biasanya dapat diterbalikkan. Interaksi ini harus dipertimbangkan pada pesakit yang mengambil etorikoksib bersamaan dengan perencat ACE atau antagonis reseptor angiotensin II. Oleh itu, kombinasi harus diberikan dengan berhati-hati, terutama pada pasien tua.
Asid asetilsalisilat: dalam kajian pada individu yang sihat, dalam keadaan stabil, etoricoxib 120 mg sekali sehari tidak memberi kesan terhadap aktiviti antiplatelet asid asetilsilatilat (81 mg sekali sehari). Etoricoxib boleh digunakan bersama dengan asid asetilsalisilat pada dos yang digunakan untuk profilaksis kardiovaskular (asid asetilsalisilat dosis rendah). Walau bagaimanapun, pemberian asid acetylsalicylic dosis rendah bersamaan dengan etoricoxib boleh mengakibatkan peningkatan kejadian ulserasi saluran gastrointestinal atau komplikasi lain berbanding dengan etoricoxib sahaja. Pemberian bersama etoricoxib dengan dos asid acetylsalicylic lebih tinggi daripada yang dijelaskan di atas untuk profilaksis kardiovaskular atau dengan NSAID lain tidak digalakkan (lihat bahagian 5.1 dan 4.4).
Ciclosporin dan tacrolimus: Walaupun interaksi ini belum dipelajari dengan etoricoxib, pemberian siklosporin atau tacrolimus bersamaan dengan NSAID jenis apa pun boleh meningkatkan kesan nefrotoksik siklosporin atau tacrolimus. Fungsi ginjal harus dipantau ketika etoricoxib diberikan dengan salah satu ubat ini.
Interaksi farmakokinetik
Kesan etorikoksib pada farmakokinetik ubat lain
Lithium: NSAID mengurangkan perkumuhan litium renal dan seterusnya meningkatkan kepekatan litium plasma. Sekiranya perlu, pantau tahap litium darah dengan teliti dan atur dos litium semasa pengambilan ubat bersamaan dan ketika rawatan dengan NSAID terganggu.
Methotrexate: dua kajian menilai kesan etoricoxib 60, 90 atau 120 mg sekali sehari selama tujuh hari pada pesakit yang menerima artritis reumatoid dengan dos methotrexate 7.5 hingga 20 mg sekali seminggu. Etoricoxib pada dos 60 dan 90 mg tidak mempengaruhi kepekatan metotreksat plasma atau pembersihan buah pinggang. Dalam satu kajian, etoricoxib 120 mg tidak berpengaruh tetapi dalam kajian lain, etoricoxib 120 mg meningkatkan kepekatan plasma methotrexate sebanyak 28% dan mengurangkan pelepasan metotreksat ginjal sebanyak 13%. Pengawasan yang mencukupi untuk ketoksikan disyorkan. Dari methotrexate apabila ditadbir bersama dengan methotrexate dan etoricoxib.
Kontraseptif oral: etoricoxib 60 mg diberikan bersama dengan kontraseptif oral yang mengandungi 35 mcg etinilestradiol (EE) dan 0,5 - 1 mg norethindrone selama 21 hari meningkatkan AUC0-24h EE keadaan tetap sebanyak 37%. Etoricoxib 120 mg bersama-sama dengan pil perancang yang sama atau dalam pentadbiran yang berasingan dengan jarak 12 jam, meningkatkan AUC0-24h EE keadaan tetap dari 50 hingga 60%. Peningkatan kepekatan EE ini harus dipertimbangkan ketika memilih oral kontraseptif untuk digunakan dengan etoricoxib. Peningkatan pendedahan EE dapat meningkatkan kejadian kejadian buruk yang berkaitan dengan kontraseptif oral (misalnya kejadian tromboemboli vena pada wanita yang berisiko).
HRT: Pentadbiran etoricoxib 120 mg dengan terapi penggantian hormon berasaskan estrogen konjugasi (0,625 mg PREMARIN) selama 28 hari meningkatkan purata AUC0-24h keadaan stabil estrone tidak terkonjugasi (41%), equilin (76%), dan 17-β- estradiol (22%). Kesan etorikoksib dosis kronik yang disyorkan (30, 60, dan 90 mg) belum dikaji. Kesan etorikoksib 120 mg terhadap pendedahan (AUC0-24h) kepada komponen estrogenik PREMARIN di atas kurang daripada separuh kesannya. diperhatikan dengan pemberian PREMARIN sahaja dan dosnya meningkat dari 0.625 hingga 1.25 mg. Kepentingan klinikal kenaikan ini tidak diketahui, dan dos PREMARIN yang lebih tinggi belum dikaji dalam kombinasi dengan etoricoxib. Peningkatan kepekatan estrogen seperti itu harus dipertimbangkan ketika memilih terapi penggantian hormon pascamenopause untuk digunakan dengan etoricoxib kerana peningkatan pendedahan kepada estrogen dapat meningkatkan risiko kejadian buruk yang berkaitan dengan HRT.
Prednisone / prednisolone: dalam kajian interaksi ubat, etoricoxib tidak mempunyai kesan yang relevan secara klinikal terhadap farmakokinetik prednisone / prednisolon.
Digoxin: etoricoxib 120 mg sekali sehari selama 10 hari kepada sukarelawan yang sihat tidak mengubah AUC0-24h keadaan stabil plasma atau "penghapusan digoxin buah pinggang. C" adalah peningkatan Cmax digoxin (kira-kira 33%). Peningkatan ini secara amnya tidak relevan bagi kebanyakan pesakit. Walau bagaimanapun, pesakit yang berisiko tinggi untuk ketoksikan digoxin harus dipantau untuk bersama-sama etoricoxib dan digoxin.
Kesan etorikoksib pada ubat yang dimetabolisme oleh sulfotransferases
Etoricoxib adalah penghambat aktiviti sulfotransferase manusia, terutamanya SULT1E1, dan telah terbukti meningkatkan kepekatan etinilestradiol dalam serum. Walaupun pengetahuan mengenai kesan beberapa sulphotransferases pada masa ini terhad dan akibat klinikal bagi banyak ubat masih dalam penyelidikan, mungkin berhati-hati ketika bersama-sama memberikan etoricoxib dengan ubat lain yang dimetabolisme terutamanya oleh sulphotransferases manusia (misalnya salbutamol dan minoxidil per os ).
Kesan etoricoxib pada ubat yang dimetabolisme oleh isoenzim sistem CYP
Berdasarkan kajian dalam vitro, etoricoxib tidak diharapkan dapat menghalang sitokrom P450 (CYP) 1A2, 2C9, 2C19, 2D6, 2E1 atau 3A4. Dalam kajian pada subjek yang sihat, pemberian etoricoxib 120 mg setiap hari tidak mengubah aktiviti hati CYP3A4 seperti yang diukur dengan ujian nafas eritromisin.
Kesan ubat lain pada farmakokinetik etoricoxib
Laluan metabolik utama etoricoxib bergantung pada enzim CYP. CYP3A4 nampaknya menyumbang kepada metabolisme etoricoxib dalam vivo. Pendidikan secara in vitro menunjukkan bahawa CYP2D6, CYP2C9, CYP1A2 dan CYP2C19 juga dapat menjadi pemangkin laluan metabolik utama, tetapi peranan kuantitatif mereka belum dipelajari dalam Saya tinggal.
Ketokonazol: ketoconazole, perencat CYP3A4 yang kuat, sekali sehari 400 mg selama 11 hari kepada sukarelawan yang sihat, tidak mempunyai kesan yang relevan secara klinikal terhadap farmakokinetik dos tunggal 60 mg etoricoxib (peningkatan AUC sebanyak 43%).
Voriconazole dan Miconazole: pemberian bersamaan oral oral voriconazole atau topikal miconazole oral, perencat kuat CYP3A4, dengan etoricoxib menyebabkan sedikit peningkatan pendedahan etoricoxib, tetapi tidak dianggap signifikan secara klinikal berdasarkan data yang diterbitkan.
Rifampisin: Pemberian etorikoksib bersamaan dengan rifampicin, pemicu kuat enzim CYP, mengakibatkan penurunan kepekatan etorikoksib plasma sebanyak 65%. Interaksi ini boleh mengakibatkan kekambuhan gejala apabila etoricoxib diberikan bersama rifampicin. Walaupun ini mungkin menunjukkan peningkatan dos, dos etoricoxib lebih tinggi daripada yang dijangkakan untuk setiap indikasi belum dipelajari dalam kombinasi dengan rifampisin dan oleh itu tidak disarankan (lihat bahagian 4.2).
Antasid: antasid tidak mempengaruhi farmakokinetik etoricoxib secara signifikan secara klinikal.
04.6 Kehamilan dan penyusuan
Kehamilan
Tidak ada data klinikal mengenai pendedahan etorikoksib pada wanita hamil. Kajian pada haiwan menunjukkan ketoksikan pembiakan (lihat bahagian 5.3). Potensi risiko pada wanita hamil tidak diketahui. Etoricoxib, seperti produk ubat lain yang menghalang sintesis prostaglandin, boleh menyebabkan rahim inersia dan penutupan prematur saluran arteri semasa trimester terakhir. Etoricoxib dikontraindikasikan pada kehamilan (lihat bahagian 4.3). Sekiranya kehamilan berlaku semasa rawatan, terapi etoricoxib harus dihentikan.
Masa makan
Tidak diketahui sama ada etoricoxib diekskresikan dalam susu manusia. Etoricoxib diekskresikan dalam susu tikus. Wanita yang mengambil etoricoxib tidak boleh menyusui (lihat bahagian 4.3 dan 5.3).
Kesuburan
Penggunaan etoricoxib, seperti bahan farmakologi lain yang diketahui menghalang COX-2, tidak digalakkan pada wanita yang merancang untuk hamil.
04.7 Kesan terhadap kemampuan memandu dan menggunakan mesin
Pesakit yang mengalami pening, vertigo atau mengantuk ketika mengambil etoricoxib harus menahan diri dari memandu atau mengendalikan mesin.
04.8 Kesan yang tidak diingini
Ringkasan profil keselamatan
Dalam kajian klinikal, etoricoxib dinilai untuk keselamatan pada 7.152 individu, termasuk 4.614 pesakit dengan OA, RA, sakit belakang kronik atau spondylitis ankylosing (kira-kira 600 pesakit dengan OA atau RA dirawat selama satu tahun atau lebih).
Dalam kajian klinikal, profil kesan yang tidak diingini serupa pada pesakit OA atau RA yang dirawat dengan etoricoxib selama satu tahun atau lebih.
Dalam kajian klinikal pada arthritis gout akut, pesakit diberi etoricoxib 120 mg sekali sehari selama 8 hari. Profil pengalaman buruk dalam kajian ini umumnya serupa dengan hasil gabungan yang dilaporkan dalam kajian OA, RA dan sakit belakang. Kronik.
Dalam program kajian keselamatan kardiovaskular berdasarkan hasil, di mana data kumpulan dari tiga percubaan yang dikendalikan pembanding aktif dinilai, 17,412 pesakit dengan OA atau RA dirawat dengan etoricoxib (60 mg atau 90 mg) untuk jangka masa purata kira-kira 18 bulan. Data keselamatan dan perincian dari kajian ini disajikan dalam bahagian 5.1.
Dalam kajian klinikal pada sakit gigi pasca operasi akut setelah pembedahan yang merangkumi 614 pesakit yang dirawat dengan etoricoxib (90 mg atau 120 mg), profil pengalaman buruk dalam kajian ini umumnya serupa dengan yang dilaporkan dalam kajian OA, AR., Dan rendah kronik sakit belakang.
Jadual tindak balas buruk
Kesan yang tidak diingini berikut dilaporkan dalam ujian klinikal, dengan "kejadian lebih tinggi daripada plasebo pada pesakit dengan OA, RA, sakit punggung kronik atau spondylitis ankylosing yang dirawat dengan etoricoxib 30 mg, 60 mg atau 90 mg hingga dos yang disyorkan sehingga pada 12 minggu; dalam kajian program MEDAL hingga 3½ tahun, dalam kajian kesakitan akut jangka pendek hingga 7 hari; atau dalam pengalaman selepas pemasaran (lihat Jadual 1):
Jadual 1:
Kesan yang tidak diingini yang serius berikut telah dilaporkan berkaitan dengan penggunaan NSAID dan tidak dapat dikecualikan dengan etoricoxib: nefrotoksisiti termasuk nefritis interstisial, sindrom nefrotik.
04.9 Overdosis
Dalam kajian klinikal, dos tunggal etoricoxib hingga 500 mg dan pelbagai dos hingga 150 mg / hari selama 21 hari tidak menyebabkan keracunan yang ketara. Terdapat laporan overdosis akut dengan etoricoxib, walaupun tidak ada pengalaman buruk yang dilaporkan dalam kebanyakan kes. Pengalaman buruk yang paling kerap diperhatikan adalah selaras dengan profil keselamatan etoricoxib (mis., Kejadian gastrointestinal, kejadian kardiorenal).
Sekiranya berlaku overdosis, adalah wajar untuk mengambil langkah-langkah sokongan yang biasa, seperti mengeluarkan bahan yang tidak diserap dari saluran pencernaan, memantau pesakit secara klinikal dan melancarkan rawatan sokongan jika perlu.
Etoricoxib tidak dapat dialisis oleh hemodialisis; tidak diketahui sama ada etoricoxib dialisis melalui dialisis peritoneal.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapeutik: ubat anti-radang dan antirheumatik, bukan steroid, coxibs.
Kod ATC: M01 AH05.
Mekanisme tindakan
Etoricoxib adalah perencat selektif siklooksigenase 2 (COX-2) dalam julat dos klinikal, untuk pemberian oral.
Dalam semua kajian farmakologi klinikal, EXINEF menghasilkan perencatan bergantung kepada dos COX-2 tanpa penghambatan COX-1 pada dos hingga 150 mg / hari. Etoricoxib tidak menghalang sintesis prostaglandin gastrik dan tidak mempengaruhi fungsi platelet.
Cyclooxygenase bertanggungjawab untuk pengeluaran prostaglandin. Dua isoform telah dikenal pasti, COX-1 dan COX-2. COX-2 adalah "isoform" enzim yang telah terbukti disebabkan oleh rangsangan proinflamasi dan diyakini bertanggungjawab terutamanya untuk sintesis mediator prostanoid kesakitan, keradangan dan demam. COX-2 juga terlibat dalam ovulasi, dalam implantasi embrio dan penutupan saluran arteri, dalam pengaturan fungsi ginjal dan dalam beberapa fungsi sistem saraf pusat (induksi demam, persepsi kesakitan dan fungsi kognitif). Ia juga dapat berperanan dalam penyembuhan ulser. COX-2 telah dikenal pasti dalam tisu di sekitar ulser gastrik pada manusia tetapi relevansinya dalam penyembuhan ulser belum diketahui.
Keberkesanan dan keselamatan klinikal
Keberkesanan
Pada pesakit dengan osteoartritis (OA), etoricoxib 60 mg sekali sehari menghasilkan peningkatan yang ketara dalam kesakitan dan penilaian pesakit terhadap status penyakit. Kesan positif ini dilihat pada awal hari kedua terapi dan berlangsung sehingga 52 minggu. Kajian dengan etoricoxib 30 mg sekali sehari menunjukkan keberkesanan unggul terhadap plasebo selama tempoh rawatan 12 minggu (menggunakan penilaian yang serupa dengan kajian di atas). Dalam kajian dos, etoricoxib 60 mg menunjukkan peningkatan yang jauh lebih besar daripada 30 mg pada ketiga-tiga primer titik akhir dalam tempoh rawatan selama 6 minggu. Dos 30 mg belum dikaji pada osteoartritis tangan.
Pada pesakit dengan rheumatoid arthritis (RA), etoricoxib 90 mg sekali sehari menghasilkan peningkatan yang ketara dalam kesakitan, keradangan dan mobiliti. Kesan positif ini dikekalkan sepanjang tempoh rawatan 12 minggu.
Pada pesakit dengan serangan artritis gout akut, etoricoxib 120 mg sekali sehari untuk tempoh rawatan selama lapan hari memberikan kelegaan dan keradangan sendi yang sederhana hingga cukup besar berbanding dengan indometasin 50 mg tiga kali sehari. Melegakan kesakitan dilihat seawal empat jam selepas memulakan rawatan.
Pada pesakit dengan spondylitis ankylosing, etoricoxib 90 mg sekali sehari memberikan peningkatan yang ketara dalam sakit tulang belakang, keradangan, kekakuan dan fungsi. Manfaat klinikal terapi etoricoxib dilihat pada hari kedua terapi dan dikekalkan sepanjang 52 minggu rawatan.
Dalam kajian klinikal yang menilai kesakitan gigi pasca operasi, etoricoxib 90 mg diberikan sekali sehari sehingga tiga hari.Pada subkumpulan pesakit dengan kesakitan sederhana pada awal, etoricoxib 90 mg menunjukkan kesan analgesik yang serupa dengan ibuprofen 600 mg (16.11 vs 16.39; P = 0.722), dan lebih tinggi daripada parasetamol / codeine 600 mg / 60 mg ( 11.00; P
Keselamatan
Program MEDAL (Etoricoxib dan Diclofenac Arthritis Multinasional Jangka Panjang)
Program MEDAL adalah program pengajian prospektif pada hasil keselamatan kardiovaskular (CV) dari kumpulan data dari tiga ujian klinikal terkawal rawak, double-blind, aktif yang dikendalikan, ujian MEDAL, EDGE II, dan EDGE.
Kajian MEDAL adalah kajian mengenai hasil CV dijalankan pada 17,804 pesakit dengan OA dan 5,700 pesakit RA yang dirawat dengan etoricoxib 60 (OA) atau 90 mg (OA dan RA) atau diclofenac 150 mg / hari untuk jangka masa 20.3 bulan (maksimum 42.3 bulan, median 21,3 bulan) . Hanya kejadian buruk dan penghentian yang disebabkan oleh sebarang kejadian buruk yang direkodkan dalam kajian ini.
Kajian EDGE dan EDGE II membandingkan toleransi gastrointestinal etoricoxib vs diclofenac. Kajian EDGE merangkumi 7.111 pesakit dengan OA yang dirawat dengan dos etoricoxib 90 mg / hari (1.5 kali dos yang disyorkan untuk OA) atau diclofenac 150 mg / hari untuk jangka masa 9.1 bulan (maksimum 16, 6 bulan, median 11.4 bulan ). Kajian EDGE II merangkumi 4.086 pesakit RA yang dirawat dengan etoricoxib 90 mg / hari atau diclofenac 150 mg / hari selama 19.2 bulan (maksimum 33.1 bulan, median 24 bulan).
Dalam program data gabungan MEDAL, 34.701 pesakit dengan OA atau RA dirawat selama 17.9 bulan (maksimum 42.3 bulan, median 16.3 bulan), dengan kira-kira 12.800 pesakit dirawat selama lebih dari 24 bulan. Pesakit yang mendaftar dalam Program ini mempunyai banyak julatfaktor risiko kardiovaskular dan gastrousus pada peringkat awal. Pesakit dengan sejarah baru infark miokard, cangkok bypass arteri koronari atau PCI dalam tempoh 6 bulan sebelum pendaftaran dikeluarkan. Penggunaan ejen gastroprotektif dan aspirin dosis rendah dibenarkan dalam kajian.
Keselamatan global:
Tidak terdapat perbezaan yang signifikan antara kadar kejadian trombotik kardiovaskular etoricoxib dan kadar diclofenac. Kejadian kardiorenal diperhatikan lebih kerap dengan etoricoxib daripada dengan diclofenac, dan kesan ini bergantung kepada dos (lihat hasil khusus di bawah). Kejadian gastrointestinal dan hepatik diperhatikan lebih kerap dengan diclofenac berbanding etoricoxib. Kejadian pengalaman buruk di EDGE dan EDGE II dan pengalaman buruk yang dianggap serius atau mungkin menyebabkan penghentian dalam kajian MEDAL lebih tinggi dengan etoricoxib berbanding dengan diclofenac.
Hasil Keselamatan Kardiovaskular:
Kejadian kejadian buruk kardiovaskular trombotik yang disahkan (kejadian vaskular jantung, serebrovaskular dan periferal) adalah setanding antara etoricoxib dan diclofenac, dan data diringkaskan dalam jadual di bawah. Tidak ada perbezaan yang signifikan secara statistik dalam kejadian kejadian trombotik dengan etoricoxib dan diclofenac di semua subkumpulan yang dianalisis termasuk semua kategori pesakit dengan risiko kardiovaskular awal. Risiko relatif untuk kejadian kardiovaskular trombotik serius yang disahkan dipertimbangkan secara berasingan dengan etoricoxib 60 mg atau 90 mg berbanding diclofenac 150 mg adalah serupa.
Kematian CV dan kematian keseluruhan adalah serupa antara kumpulan rawatan etoricoxib dan diclofenac.
Kejadian kardiorenal:
Kira-kira 50% pesakit yang mendaftar dalam kajian MEDAL mempunyai sejarah hipertensi pada peringkat awal. Dalam kajian ini, kejadian penghentian akibat kejadian buruk yang berkaitan dengan hipertensi secara statistik lebih tinggi untuk etorikoksib daripada diclofenac. Kejadian kejadian buruk untuk kegagalan jantung kongestif (gangguan dan kejadian serius) berlaku pada kadar yang sama dengan etoricoxib 60 mg berbanding diclofenac 150 mg, tetapi lebih tinggi untuk etoricoxib 90 mg daripada diclofenac 150 mg (signifikan secara statistik untuk etoricoxib 90 mg vs diclofenac 150 mg dalam kohort MEDAL OA). Kejadian kejadian buruk yang disahkan untuk kegagalan jantung kongestif (kejadian serius yang membawa ke hospital atau lawatan jabatan kecemasan) jauh lebih tinggi. Tidak signifikan dengan etoricoxib berbanding diclofenac 150 mg, dan kesan ini adalah dos -bergantungan. Kejadian pemberhentian akibat kejadian buruk yang berkaitan dengan edema lebih tinggi untuk etoricoxib daripada diclofenac 150 mg, dan kesan ini bergantung kepada dos (signifikan secara statistik untuk etoricoxib 90 mg, tetapi tidak untuk etoricoxib 60 mg).
Hasil kardiorenal untuk EDGE dan EDGE II sesuai dengan yang dijelaskan untuk kajian MEDAL.
Dalam kajian individu program MEDAL, kejadian mutlak penghentian dalam semua kumpulan rawatan untuk etoricoxib (60 mg atau 90 mg) adalah hingga 2,6% untuk hipertensi, hingga 1,9% untuk edema, dan hingga 1,1% untuk kegagalan jantung kongestif , dengan kadar penghentian yang lebih tinggi diperhatikan dengan etoricoxib 90 mg berbanding etoricoxib 60 mg.
Hasil toleransi gastrousus dari program MEDAL:
Dalam setiap tiga kajian bahagian program MEDAL, kadar penghentian yang jauh lebih rendah diperhatikan untuk etoricoxib daripada diclofenac untuk semua kejadian klinikal buruk GI (mis., Dispepsia, sakit perut, ulser). Penghentian kerana kejadian klinikal buruk GI per 100 pesakit-tahun selama keseluruhan tempoh kajian adalah seperti berikut: 3.23 untuk etoricoxib dan 4.96 untuk diclofenac dalam kajian MEDAL; 9.12 dengan etoricoxib dan 12.28 dengan diclofenac dalam kajian EDGE; dan 3.71 dengan etoricoxib dan 4.81 dengan diclofenac dalam kajian EDGE II.
Hasil keselamatan gastrousus dari program MEDAL:
Kejadian GI atas didefinisikan sebagai perforasi, bisul dan pendarahan. Subset dari semua kejadian GI atas yang dianggap rumit merangkumi perforasi, halangan, dan pendarahan yang rumit; subset kejadian GI atas yang dianggap tidak rumit termasuk pendarahan yang tidak rumit dan bisul yang tidak rumit. Kadar kejadian GI keseluruhan yang jauh lebih rendah diperhatikan dengan etoricoxib berbanding dengan diclofenac. Tidak ada perbezaan yang signifikan antara etoricoxib dan diclofenac berkenaan dengan kadar kejadian yang rumit. Untuk subkumpulan kejadian pendarahan GI atas (gabungan data rumit dan tidak rumit), tidak ada perbezaan yang signifikan antara etoricoxib dan diclofenac. Pada pesakit dengan terapi aspirin dosis rendah bersamaan (kira-kira 33% pesakit) tidak ada faedah yang signifikan dengan etoricoxib diclofenac di saluran GI atas.
Kadar per 100 pesakit-tahun untuk kejadian GI atas yang rumit dan tidak rumit (perforasi, ulser dan pendarahan (PUB)) adalah 0.67 (95% CI 0.57, 0.77) dengan etoricoxib dan 0.97 (95% CI 0.85, 1.10) dengan diclofenac, mengakibatkan risiko relatif 0.69 (95% CI 0.57, 0.83).
Kadar kejadian GI atas yang disahkan pada pesakit tua dinilai dan penurunan terbesar dilihat pada pesakit ≥ 75 tahun, 1.35 [95% CI 0.94, 1.87] vs. 2.78 [95% CI 2.14, 3.56] peristiwa setiap 100 pesakit-tahun untuk etoricoxib dan diclofenac, masing-masing.
Kadar kejadian klinikal yang disahkan mempengaruhi saluran GI bawah (perforasi, penyumbatan atau pendarahan usus kecil atau besar (POB)), tidak berbeza secara signifikan antara etoricoxib dan diclofenac.
Hasil keselamatan hepatik program MEDAL:
Etoricoxib dikaitkan dengan kadar penghentian yang jauh lebih rendah disebabkan oleh pengalaman buruk hepatik daripada diclofenac. Dalam data gabungan dari program MEDAL, 0.3% pesakit yang menerima etoricoxib dan 2.7% pesakit yang menerima diclofenac berhenti kerana kejadian buruk hepatik.
Kadar per 100 pesakit-tahun adalah 0.22 untuk etoricoxib dan 1.84 untuk diclofenac (nilai p adalah
Data keselamatan tambahan yang berkaitan dengan kejadian trombotik kardiovaskular
Dalam ujian klinikal tidak termasuk kajian program MEDAL, kira-kira 3,100 pesakit dirawat etoricoxib ≥60 mg / hari selama 12 minggu atau lebih. Tidak ada perbezaan yang ketara dalam kadar kejadian kardiovaskular trombotik yang disahkan serius antara pesakit yang dirawat dengan etoricoxib ≥60 mg, plasebo, atau NSAID tidak termasuk naproxen. Walau bagaimanapun, kejadian kejadian ini lebih tinggi pada pesakit yang dirawat dengan etoricoxib daripada yang dirawat dengan naproxen 500 mg dua kali sehari. Perbezaan aktiviti antiplatelet antara beberapa NSAID inhibitor COX-1 dan inhibitor selektif COX-2 boleh mempengaruhi kepentingan klinikal pada pesakit di risiko untuk kejadian tromboemboli COX-2 inhibitor mengurangkan pembentukan prostacyclin sistemik (dan oleh itu mungkin endotelel) tanpa mempengaruhi tromboksana platelet. Perkaitan klinikal penemuan ini belum dapat dipastikan.
Data keselamatan gastrousus tambahan
Dalam dua kajian endoskopi double-blind 12 minggu, kejadian kumulatif ulser gastrointestinal jauh lebih rendah pada pesakit yang dirawat dengan etoricoxib 120 mg sekali sehari berbanding pesakit yang dirawat dengan naproxen 500 mg dua kali sehari atau ibuprofen 800 mg tiga kali sehari Etoricoxib mempunyai kejadian ulser gastrousus yang lebih tinggi daripada plasebo.
Kajian fungsi ginjal pada orang tua
Kesan rawatan selama 15 hari dengan etoricoxib (90 mg), celecoxib (200 mg bid), naproxen (500 mg bid) dan plasebo pada perkumuhan natrium kencing, tekanan darah, dan parameter fungsi ginjal lain pada subjek berusia 60 dan 85 tahun pada rejimen diet 200 mEq / hari natrium, dinilai dalam kajian kumpulan selari secara rawak, double-blind, plasebo. Etoricoxib, celecoxib, dan naproxen mempunyai kesan yang sama terhadap perkumuhan natrium kencing selama 2 minggu rawatan. Semua pembanding aktif menunjukkan peningkatan nilai tekanan darah sistolik berbanding dengan plasebo; namun, etoricoxib dikaitkan dengan peningkatan. Signifikan secara statistik pada hari ke-14 berbanding dengan celecoxib dan naproxen (perubahan min dari awal untuk tekanan darah sistolik: etoricoxib 7,7 mmHg, celecoxib 2,4 mmHg, naproxen 3,6 mmHg).
05.2 Sifat farmakokinetik
Penyerapan
Etorikoksib yang diberikan secara oral diserap dengan baik. Purata ketersediaan bio selepas pemberian oral adalah sekitar 100%. Dengan pemberian sekali sehari sebanyak 120 mg, kepekatan plasma puncak (min geometri Cmax = 3.6 μg / ml) Keadaan stabil diperhatikan kira-kira 1 jam (Tmax) selepas dos pada orang dewasa yang berpuasa.Rata-rata geometri kawasan di bawah lengkung (AUC0-24h) ialah 37.8 mcg • j / ml. Farmakokinetik etoricoxib adalah linear di seluruh spektrum dos klinikal.
Pengambilan makanan (makanan berlemak tinggi) tidak mempengaruhi tahap penyerapan daripada etoricoxib 120 mg. Kadar penyerapan diubah, dengan penurunan Cmax sebanyak 36% dan peningkatan Tmax selama dua jam. Data ini tidak dianggap signifikan secara klinikal.Dalam kajian klinikal, etoricoxib diberikan tanpa mengambil kira makanan.
Pembahagian
Etoricoxib kira-kira 92% terikat dengan protein plasma manusia pada kepekatan antara 0,05 hingga 5 mcg / ml. Pada manusia, jumlah taburan keadaan tetap (Vdss) adalah kira-kira 120 l.
Etoricoxib melintasi plasenta pada tikus dan arnab, dan penghalang otak darah pada tikus.
Metabolisme
Etoricoxib dimetabolisme secara meluas dalam air kencing sebagai ubat induk. Jalur metabolik utama untuk pembentukan turunan 6-hidroksimetil dikatalisis oleh enzim CYP. CYP3A4 nampaknya menyumbang kepada metabolisme etoricoxib. dalam vivo. Kajian in vitro menunjukkan bahawa CYP2D6, CYP2C9, CYP1A2 dan CYP2C19 juga boleh menjadi pemangkin laluan metabolik utama, tetapi peranan kuantitatif mereka belum dipelajari. dalam vivo.
Lima metabolit telah dikenal pasti pada manusia. Metabolit utama adalah turunan asid karboksilat 6 "etoricoxib yang terbentuk oleh" pengoksidaan selanjutnya dari turunan 6 "hidroksimetil. Metabolit utama ini sama ada tidak menunjukkan aktiviti yang dapat diukur atau hanya menunjukkan aktiviti yang lemah. Sebagai COX -2 perencat Tiada metabolit ini menghalang COX-1.
Penghapusan
Berikutan pemberian etoricoxib radiolabel 25 mg dos intravena tunggal kepada subjek yang sihat, 70% radioaktiviti dikesan dalam air kencing dan 20% pada najis, kebanyakannya dalam bentuk metabolit. Kurang daripada 2% didapati sebagai ubat yang tidak berubah.
Penghapusan etorikoksib berlaku hampir secara eksklusif melalui metabolisme diikuti oleh perkumuhan buah pinggang. Kepekatan etorikoksib dalam keadaan stabil dicapai dalam masa tujuh hari dengan pemberian sekali sehari 120 mg, dengan kadar pengumpulan kira-kira 2, bersamaan dengan waktu hayat pengumpulan kira-kira 22 jam. Pelepasan plasma dianggarkan sekitar 50 ml / min setelah dos intravena 25 mg.
Ciri-ciri pesakit
Warga emasFarmakokinetik pada orang tua (berumur 65 tahun dan lebih tua) serupa dengan yang ada pada golongan muda.
Seks: farmakokinetik etoricoxib serupa pada lelaki dan wanita.
Kekurangan hepatik: Pada pesakit dengan disfungsi hepatik ringan (skor Child-Pugh 5-6) pemberian etorikoksibib 60 mg sekali sehari menghasilkan AUC rata-rata sekitar 16% lebih tinggi daripada pada subjek sihat yang diberi dos yang sama. Pada pesakit dengan disfungsi hepatik sederhana (skor Child-Pugh 7-9) diberikan 60 mg etoricoxib setiap hari lain, Maksud AUC adalah serupa dengan subjek yang sihat yang diberikan etoricoxib 60 mg sekali sehari; etoricoxib 30 mg sekali sehari belum dipelajari dalam populasi ini. Tidak ada data klinikal atau farmakokinetik pada pesakit dengan disfungsi teruk. Hati (skor Child-Pugh ≥10), (lihat bahagian 4.2 dan 4.3).
Kegagalan buah pinggang: Farmakokinetik dosis etoricoxib 120 mg tunggal pada pesakit dengan gangguan buah pinggang sederhana hingga teruk dan pada pesakit hemodialisis dengan penyakit ginjal tahap akhir tidak jauh berbeza dengan subjek sihat. Hemodialisis menyumbang kepada penghapusan (pelepasan dialisis kira-kira 50 ml / min) (lihat bahagian 4.3 dan 4.4).
Pesakit kanak-kanak: farmakokinetik etoricoxib pada pesakit kanak-kanak (
Dalam kajian farmakokinetik (n = 16) yang dilakukan pada remaja (umur 12-17), farmakokinetik pada remaja dengan berat 40 hingga 60 kg dirawat dengan etoricoxib 60 mg sekali sehari dan remaja> 60 kg yang dirawat dengan etoricoxib 90 mg sekali sehari adalah serupa dengan pada orang dewasa yang dirawat dengan etoricoxib 90 mg sekali sehari. Keselamatan dan keberkesanan etoricoxib pada pesakit pediatrik belum terbukti (lihat bahagian 4.2).
05.3 Data keselamatan praklinikal
Dalam kajian praklinik, etorikoksib terbukti tidak genotoksik. Etorikoksib tidak karsinogenik pada tikus. Tikus dirawat setiap hari selama lebih kurang dua tahun pada dos> 2 kali ganda dos harian manusia [90 mg] berdasarkan pendedahan sistemik mengembangkan adenoma hepatoselular dan adenoma folikel kelenjar tiroid.Tumor jenis ini yang diperhatikan pada tikus dianggap sebagai konsekuensi spesies spesifik dari induksi enzim CYP hepatik pada tikus. Etoricoxib belum terbukti dapat menyebabkan induksi enzim CYP3A hepatik pada manusia.
Pada tikus, ketoksikan gastrointestinal etoricoxib meningkat dengan dos dan masa pendedahan. Dalam kajian ketoksikan tikus selama 14 minggu, etoricoxib menyebabkan ulser gastrointestinal pada dos melebihi dos terapi manusia. Dalam kajian ketoksikan selama 53- dan 106 minggu, ulser gastrointestinal juga diperhatikan pada pendedahan yang setanding dengan yang diperhatikan pada manusia pada dos terapeutik.Pada pendedahan tinggi, perubahan ginjal dan gastrointestinal diperhatikan pada anjing.
Etoricoxib tidak teratogenik dalam kajian ketoksikan pembiakan yang dilakukan pada tikus pada kadar 15 mg / kg / hari (pendedahan kira-kira 1.5 kali dos harian manusia [90 mg] berdasarkan pendedahan sistemik). Pada arnab, peningkatan berkaitan dengan dos dalam malformasi kardiovaskular diperhatikan pada tahap pendedahan di bawah pendedahan klinikal yang dapat dicapai pada manusia pada dos harian (90 mg). Walau bagaimanapun, tidak ada kerangka janin atau kelainan luaran yang berkaitan dengan rawatan yang diperhatikan. Pada tikus dan arnab, terdapat peningkatan berkaitan dengan dos dalam kehilangan pasca implantasi pada pendedahan yang lebih besar daripada atau sama dengan 1.5 kali pendedahan manusia (lihat bahagian 4.3 dan 4.6).
Etoricoxib diekskresikan dalam susu tikus yang menyusui pada kepekatan kira-kira dua kali ganda daripada plasma. Terdapat penurunan berat badan pada anak yang terdedah kepada susu dari haiwan menyusui yang dirawat dengan etoricoxib.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Di dalam tablet:
Kalsium fosfat dibasik anhidrat
Natrium Croscarmellose
Magnesium stearat
Selulosa mikrokristalin
Salutan tablet:
Lilin Carnauba
Laktosa monohidrat
Hypromellose
Titanium dioksida (E171)
Triacetin
Tablet 30, 60 dan 120 mg juga mengandungi tasik indigo carmine (E132) dan oksida besi kuning (E172).
06.2 Ketidaksesuaian
Tidak relevan.
06.3 Tempoh sah
3 tahun.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Botol: Simpan bekas tertutup rapat untuk melindungi dari kelembapan.
Lepuh: Simpan dalam bungkusan asli untuk melindungi dari kelembapan.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
30 mg
Lepuh aluminium / aluminium dalam pek 2, 7, 14, 20, 28, 49 tablet atau pelbagai pek 98 (2 bungkus 49) tablet.
60, 90 dan 120 mg
Lepuh aluminium / aluminium dalam pek 2, 5, 7, 10, 14, 20, 28, 30, 50, 84, 100 tablet atau pelbagai pek 98 (2 bungkus 49) tablet.
Lepuh aluminium / aluminium (dos tunggal) dalam pek 50 dan 100 tablet.
Botol HDPE berwarna putih, bulat dengan penutup polipropilena putih yang mengandungi 30 tablet dengan dua bekas pengering 1 gram dan 90 tablet dengan satu bekas pengering.
Tidak semua saiz pek boleh dipasarkan.
06.6 Arahan penggunaan dan pengendalian
Tiada arahan khas.
07.0 PEMEGANG KEBENARAN PEMASARAN
Abiogen Pharma S.p.A.
Via Meucci, 36 - Ospedaletto - Pisa
08.0 NOMBOR KEBENARAN PEMASARAN
"Tablet bersalut filem 30 mg" 7 tablet dalam lepuh Al / Al AIC n.035822446 / M
"Tablet bersalut filem 30 mg" 28 tablet dalam lepuh Al / Al AIC n.035822434 / M
"Tablet bersalut filem 60 mg" 2 tablet dalam lepuh Al / Al AIC n. 035822016 / M
"Tablet bersalut filem 60 mg" 5 tablet dalam lepuh Al / Al AIC n. 035822028 / M
"Tablet bersalut filem 60 mg" 7 tablet dalam lepuh Al / Al AIC n. 035822030 / M
"Tablet bersalut filem 60 mg" 10 tablet dalam lepuh Al / Al AIC n. 035822042 / M
"Tablet bersalut filem 60 mg" 14 tablet dalam lepuh Al / Al AIC n. 035822055 / M
"Tablet bersalut filem 60 mg" 20 tablet dalam lepuh Al / Al AIC n. 035822067 / M
"Tablet bersalut filem 60 mg" 28 tablet dalam lepuh Al / Al AIC n. 035822079 / M
"Tablet bersalut filem 60 mg" 30 tablet dalam lepuh Al / Al AIC n. 035822081 / M
"Tablet bersalut filem 60 mg" 50 tablet dalam lepuh Al / Al AIC n. 035822093 / M
"Tablet bersalut filem 60 mg" tablet 98 (2x49) dalam lepuh Al / Al AIC n. 035822105 / M
"Tablet bersalut filem 60 mg" 100 tablet dalam lepuh Al / Al AIC n. 035822117 / M
"Tablet bersalut filem 60 mg" Tablet 50x1 dalam lepuh Al / Al AIC n. 035822129 / M
"Tablet bersalut filem 60 mg" Tablet 100x1 dalam lepuh Al / Al AIC n. 035822131 / M
"Tablet bersalut filem 60 mg" 30 tablet dalam botol HDPE AIC n. 035822143 / M
"Tablet bersalut filem 90 mg" 2 tablet dalam lepuh Al / Al AIC n. 035822156 / M
"Tablet bersalut filem 90 mg" 5 tablet dalam lepuh Al / Al AIC n. 035822168 / M
"90 mg tablet bersalut filem" 7 tablet dalam lepuh Al / Al AIC n. 035822170 / M
"Tablet bersalut filem 90 mg" 10 tablet dalam lepuh Al / Al AIC n. 035822182 / M
"90 mg tablet bersalut filem" 14 tablet dalam lepuh Al / Al AIC n. 035822194 / M
"Tablet bersalut filem 90 mg" 20 tablet dalam lepuh Al / Al AIC n. 035822206 / M
"Tablet bersalut filem 90 mg" 28 tablet dalam lepuh Al / Al AIC n. 035822218 / M
"Tablet bersalut filem 90 mg" 30 tablet dalam lepuh Al / Al AIC n. 035822220 / M
"Tablet bersalut filem 90 mg" 50 tablet dalam lepuh Al / Al AIC n. 035822232 / M
"90 mg tablet bersalut filem" 98 (2x49) tablet dalam lepuh Al / Al AIC n. 035822244 / M
"Tablet bersalut filem 90 mg" 100 tablet dalam lepuh Al / Al AIC n. 035822257 / M
"Tablet bersalut filem 90 mg" Tablet 50x1 dalam lepuh Al / Al AIC n. 035822269 / M
"Tablet bersalut filem 90 mg" Tablet 100x1 dalam lepuh Al / Al AIC n. 035822271 / M
"Tablet bersalut filem 90 mg" 30 tablet dalam botol HDPE AIC n. 035822283 / M
"Tablet bersalut filem 120 mg" 2 tablet dalam lepuh Al / Al AIC n. 035822295 / M
"120 mg tablet bersalut filem" 5 tablet dalam lepuh Al / Al AIC n. 035822307 / M
"120 mg tablet bersalut filem" 7 tablet dalam lepuh Al / Al AIC n. 035822319 / M
"120 mg tablet bersalut filem" 10 tablet dalam lepuh Al / Al AIC n. 035822321 / M
"120 mg tablet bersalut filem" 14 tablet dalam lepuh Al / Al AIC n. 035822333 / M
"120 mg tablet bersalut filem" 20 tablet dalam lepuh Al / Al AIC n. 035822345 / M
"120 mg tablet bersalut filem" 28 tablet dalam lepuh Al / Al AIC n. 035822358 / M
"Tablet bersalut filem 120 mg" 30 tablet dalam lepuh Al / Al AIC n. 035822360 / M
"Tablet bersalut filem 120 mg" 50 tablet dalam lepuh Al / Al AIC n. 035822372 / M
"120 mg tablet bersalut filem" 98 (2x49) tablet dalam lepuh Al / Al AIC n. 035822384 / M
"Tablet bersalut filem 120 mg" 100 tablet dalam lepuh Al / Al AIC n. 035822396 / M
"Tablet bersalut filem 120 mg" Tablet 50x1 dalam lepuh Al / Al AIC n. 035822408 / M
"Tablet bersalut filem 120 mg" Tablet 100x1 dalam lepuh Al / Al AIC n. 035822410 / M
"120 mg tablet bersalut filem" 30 tablet dalam botol HDPE AIC n. 035822422 / M
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Februari 2004 / Februari 2012
10.0 TARIKH SEMAKAN TEKS
Mei 2013