Bahan aktif: Zolmitriptan
Tablet bersalut filem Zomig 2.5 mg dan 5 mg
Sisip pakej Zomig tersedia untuk saiz pek:- Tablet bersalut filem Zomig 2.5 mg dan 5 mg
- Zomig 2.5 mg / dos dan 5 mg / dos semburan hidung, larutan
- Zomig Rapimelt 2.5 mg dan 5 mg tablet boleh disebarkan
Petunjuk Mengapa Zomig digunakan? Untuk apa itu?
Zomig mengandungi zolmitriptan dan tergolong dalam kumpulan ubat yang disebut triptans.
Zomig digunakan untuk rawatan sakit kepala migrain.
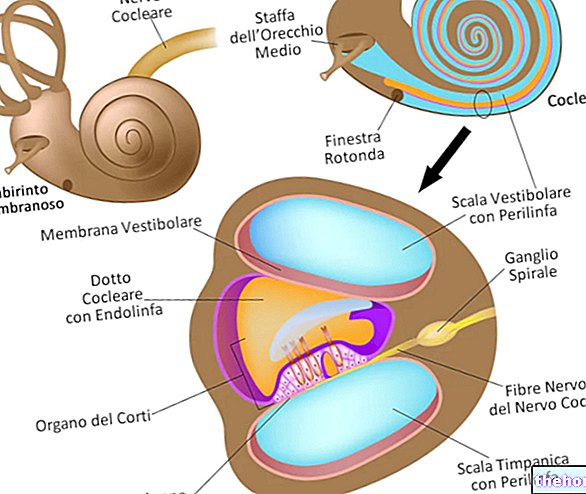
- Gejala migrain boleh disebabkan oleh pelebaran saluran darah di kepala. Zomig dipercayai dapat mengurangkan pelebaran saluran darah ini. Ini membantu melegakan sakit kepala dan gejala serangan migrain lain, seperti mual atau sakit kepala. Muntah dan kepekaan terhadap cahaya dan suara.
- Zomig hanya berfungsi apabila serangan migrain telah bermula. Ia tidak menghalang permulaan serangan
Kontraindikasi Apabila Zomig tidak boleh digunakan
Jangan ambil Zomig
- jika anda alah (hipersensitif) terhadap zolmitriptan atau mana-mana ramuan lain dari ubat ini (lihat bahagian 6: Maklumat lebih lanjut)
- jika anda mempunyai tekanan darah tinggi
- jika anda pernah mengalami masalah jantung, termasuk serangan jantung, angina (sakit dada yang disebabkan oleh senaman atau senaman), angina Prinzmetal (sakit dada yang berlaku ketika rehat) atau jika anda pernah mengalami gejala yang berkaitan dengan jantung seperti sesak nafas atau tekanan dada
- jika anda pernah mengalami strok atau simptom strok jangka pendek (serangan iskemia sementara atau TIA)
- sekiranya anda mengalami masalah buah pinggang yang teruk
- jika anda mengambil ubat migrain lain (contohnya ubat ergotamin atau jenis ergot seperti dihydroergotamine dan methysergide) atau triptan lain untuk migrain pada masa yang sama. Lihat bahagian: "Mengambil Zomig dengan ubat lain" untuk maklumat lebih lanjut.
Sekiranya ragu-ragu, berjumpa dengan doktor atau ahli farmasi anda.
Langkah berjaga-jaga untuk penggunaan Apa yang perlu anda ketahui sebelum mengambil Zomig
Sebelum mengambil Zomig, beritahu doktor anda jika:
- anda berisiko menghidap penyakit jantung iskemia (aliran darah yang lemah di arteri jantung). Risiko lebih tinggi jika anda merokok, mempunyai tekanan darah tinggi, mempunyai kadar kolesterol tinggi, menghidap diabetes, atau jika seseorang di keluarga anda menghidap penyakit jantung iskemik
- jika anda diberitahu bahawa anda menghidapi sindrom Wolff-Parkinson-White (sejenis kelainan degupan jantung)
- sekiranya anda pernah mengalami masalah hati
- jika anda mengalami sakit kepala selain daripada sakit kepala migrain biasa
- jika anda mengambil ubat untuk mengatasi kemurungan (lihat "Mengambil Zomig dengan ubat lain" di bahagian ini). Sekiranya anda dimasukkan ke hospital, beritahu kakitangan perubatan bahawa anda mengambil Zomig.
Zomig tidak digalakkan untuk orang di bawah umur 18 tahun atau lebih dari 65 tahun.
Seperti rawatan migrain lain, terlalu banyak menggunakan Zomig boleh menyebabkan sakit kepala setiap hari atau boleh membuat sakit kepala migrain bertambah buruk. Bercakap dengan doktor anda jika anda rasa ini masalahnya. Anda mungkin perlu berhenti menggunakan Zomig untuk membetulkan masalahnya.
Interaksi Dadah atau makanan mana yang boleh mengubah kesan Zomig
Beritahu doktor atau ahli farmasi anda jika anda mengambil atau baru-baru ini mengambil ubat lain termasuk ubat-ubatan herba dan ubat-ubatan yang diperoleh tanpa preskripsi
Khususnya, beritahu doktor anda jika anda mengambil salah satu ubat berikut:
Ubat untuk migrain
- Sekiranya anda mengambil triptans selain Zomig, biarkan 24 jam berlalu sebelum mengambil Zomig.
- Setelah mengambil Zomig biarkan 24 jam berlalu sebelum mengambil triptan lain selain Zomig
- Sekiranya anda mengambil ubat yang mengandungi ergotamine atau ubat jenis ergot (seperti dihydroergotamine atau methysergide), biarkan 24 jam berlalu sebelum mengambil Zomig.
- Setelah mengambil Zomig, biarkan 6 jam berlalu sebelum mengambil ubat ergotamin atau jenis ergot.
Ubat untuk kemurungan
- moclobemide atau fluvoxamine
- ubat yang dipanggil SSRI (perencat pengambilan serotonin selektif)
- ubat-ubatan yang dipanggil SNRI (serotonin dan norepinephrine reuptake inhibitor) seperti venlafaxine, duloxetine.
Ubat-ubatan lain
- cimetidine (untuk masalah pencernaan atau ulser perut)
- antibiotik quinolone (mis. ciprofloxacin)
Sekiranya anda mengambil persediaan herba yang mengandungi St. John's wort (Hypericum perforatum), anda cenderung mengalami kesan sampingan Zomig.
Menggunakan Zomig dengan makanan dan minuman
Anda boleh mengambil Zomig dengan atau tanpa makanan. Makanan tidak mempengaruhi tindakan Zomig.
Amaran Penting untuk mengetahui bahawa:
Kehamilan dan penyusuan
Tidak diketahui sama ada pengambilan Zomig semasa mengandung adalah berbahaya.Sebelum mengambil Zomig, beritahu doktor anda jika anda hamil atau cuba hamil.
Jangan menyusui selama 24 jam selepas mengambil Zomig.
Memandu dan menggunakan mesin
Semasa serangan migrain, reaksi anda mungkin lebih lambat daripada biasa. Perkara ini harus diingat semasa memandu atau menggunakan alat atau mesin.
Zomig tidak mungkin mempengaruhi kemampuan anda untuk memandu atau menggunakan alat atau mesin. Walau bagaimanapun, lebih baik menunggu untuk melihat apa kesan Zomig sebelum memulakan aktiviti ini.
Maklumat penting mengenai beberapa ramuan Zomig
Tablet Zomig mengandungi laktosa yang merupakan sejenis gula. Sekiranya anda diberitahu oleh doktor bahawa anda tidak bertoleransi atau mencerna beberapa gula (mempunyai "intoleransi terhadap beberapa gula), berjumpa dengan doktor anda sebelum mengambil ubat ini.
Dos, Kaedah dan Masa Pentadbiran Cara menggunakan Zomig: Posologi
Sentiasa ambil Zomig tepat seperti yang diberitahu oleh doktor anda. Sekiranya ragu-ragu, anda harus berjumpa doktor atau ahli farmasi anda.
Anda boleh mengambil Zomig sebaik sahaja sakit kepala migrain bermula. Ia juga dapat berlaku setelah serangan sedang dilakukan.
Dos biasa adalah satu tablet (2.5 mg atau 5 mg). • Telan tablet dengan minum air.
Anda boleh mengambil tablet lain jika migrain masih ada selepas dua jam atau jika kembali dalam 24 jam.
Sekiranya tablet ini tidak dapat membantu migrain anda, beritahu doktor anda. Doktor anda boleh meningkatkan dos menjadi 5 mg atau mengubah rawatan anda.
Jangan mengambil lebih daripada dos yang ditetapkan.
Jangan mengambil lebih daripada dua dos dalam satu hari. Sekiranya anda diberi tablet 2.5 mg, dos harian maksimum ialah 5 mg. Sekiranya anda diberi tablet 5 mg, dos harian maksimum ialah 10 mg.
Overdosis Apa yang perlu dilakukan jika anda mengambil terlalu banyak Zomig
Sekiranya anda telah mengambil lebih banyak Zomig daripada yang ditetapkan oleh doktor anda, segera hubungi doktor anda atau pergi ke hospital terdekat. Bawa Zomig dengan anda.
Kesan Sampingan Apakah kesan sampingan Zomig
Seperti semua ubat, Zomig boleh menyebabkan kesan sampingan, walaupun tidak semua orang mengalaminya.
Beberapa gejala di bawah ini boleh menjadi sebahagian daripada serangan migrain itu sendiri.
Kesan sampingan yang biasa (mempengaruhi lebih daripada 1 dari 100 orang):
- Kepekaan yang tidak normal seperti kesemutan di jari dan jari kaki atau kulit yang sensitif terhadap sentuhan
- Mengantuk, pening atau rasa panas
- Sakit kepala
- Denyutan jantung tidak teratur
- Loya
- Dia mencuba semula
- Sakit perut
- Mulut kering
- Kelemahan otot atau sakit otot
- Kelemahan
- Kesukaran, sesak, sakit atau tekanan pada tekak, leher, lengan dan kaki atau dada
- Kesukaran menelan.
Kesan sampingan yang tidak biasa (mempengaruhi kurang dari 1 dari 100 orang):
- Degupan jantung yang sangat pantas
- Tekanan darah sedikit lebih tinggi
- Peningkatan jumlah air kencing atau keperluan untuk membuang air kecil
Kesan sampingan yang jarang berlaku (mempengaruhi kurang dari 1 dalam 1,000 orang):
- Reaksi alergi / hipersensitiviti, termasuk ruam kulit (gatal-gatal) dan pembengkakan muka, bibir, mulut, lidah dan tekak. Sekiranya anda fikir Zomig menyebabkan reaksi alergi, hentikan pengambilannya dan segera hubungi doktor anda.
Kesan sampingan yang sangat jarang berlaku (mempengaruhi kurang dari 1 dalam 10,000 orang):
- Angina (sakit dada, sering disebabkan oleh senaman), serangan jantung atau kekejangan saluran darah jantung.Jika anda melihat sakit dada atau sesak nafas setelah mengambil Zomig, hubungi doktor anda dan jangan mengambil Zomig lebih lanjut.
- Kekejangan saluran darah di usus, yang boleh merosakkan usus. Anda mungkin melihat sakit perut atau cirit-birit berdarah. Sekiranya ini berlaku, hubungi doktor anda dan jangan minum Zomig lebih banyak.
Melaporkan kesan sampingan
Sekiranya anda mendapat kesan sampingan, berbincanglah dengan doktor atau ahli farmasi anda. Ini termasuk kemungkinan kesan sampingan yang tidak disenaraikan dalam risalah ini. Anda juga boleh melaporkan kesan sampingan secara langsung melalui sistem pelaporan nasional di www.agenziafarmaco.it/it/responsabili. Dengan melaporkan kesan sampingan, anda dapat membantu memberikan lebih banyak maklumat mengenai keselamatan ubat ini.
Tamat Tempoh dan Pengekalan
- Jauhkan dari jarak dan jangkauan kanak-kanak.
- Jangan gunakan Zomig selepas tarikh luput yang dinyatakan pada pek. Tarikh luput merujuk pada hari terakhir dalam sebulan.
- Jangan simpan di atas 30 ° C.
- Ubat tidak boleh dibuang melalui air sisa atau sampah isi rumah. Tanya ahli farmasi anda bagaimana membuang ubat yang tidak lagi anda gunakan. Ini akan membantu melindungi alam sekitar.
Maklumat lain
Apa yang mengandungi Zomig
- Bahan aktifnya ialah zolmitriptan. Tablet bersalut filem Zomig mengandungi 2.5 mg atau 5 mg zolmitriptan.
- Bahan-bahan lain adalah: laktosa anhidrat, selulosa mikrokristal, natrium pati glikolat (jenis A), magnesium stearat, makrogol, hypromellose, titanium dioksida (E171), oksida besi kuning (E172, hanya dalam tablet 2.5 mg), oksida besi merah (E172 , Tablet 5 mg sahaja).
Apa rupa Zomig dan kandungan peknya
- Tablet bersalut filem Zomig 2.5 mg berwarna kuning, bulat dan ditulis dengan huruf "Z" di satu sisi.
- Tablet bersalut filem Zomig 5 mg berwarna merah jambu, bulat dan ditulis dengan huruf "Z" di satu sisi.
- Tablet bersalut filem Zomig 2.5 mg dan 5 mg boleh didapati dalam lepuh yang mengandungi 3, 6 (dengan atau tanpa bekas), 12 atau 18 tablet.
Bekas itu adalah bekas plastik keras di mana anda boleh menyimpan tablet untuk kemudahan. Sekiranya anda menggunakan bekas itu, anda mesti menyimpan kadbod luar dan risalah ini kerana anda mungkin perlu merujuknya semula.
Tidak semua saiz pek boleh dipasarkan.
Risalah Pakej Sumber: AIFA (Badan Perubatan Itali). Kandungan yang diterbitkan pada Januari 2016. Maklumat yang ada mungkin tidak terkini.
Untuk mempunyai akses ke versi paling terkini, disarankan untuk mengakses laman web AIFA (Badan Perubatan Itali). Penafian dan maklumat berguna.
01.0 NAMA PRODUK PERUBATAN
TABEL ZOMIG DILAPAT DENGAN FILM
02.0 KOMPOSISI KUALITATIF DAN KUANTITATIF
Zolmitriptan.
Setiap tablet bersalut filem 2.5 mg mengandungi 2.5 mg zolmitriptan.
Setiap tablet bersalut filem 5 mg mengandungi 5 mg zolmitriptan.
Penerima:
Setiap tablet bersalut filem 2.5 mg mengandungi 100 mg laktosa.
Setiap tablet bersalut filem 5 mg mengandungi 200 mg laktosa.
Untuk senarai lengkap eksipien, lihat bahagian 6.1.
03.0 BORANG FARMASI
Tablet bersalut filem.
Tablet bersalut filem bulat, biconvex, kuning atau merah jambu yang masing-masing mengandungi 2.5 mg dan 5 mg zolmitriptan. Tablet ini ditulis dengan huruf "Z" di satu sisi.
04.0 MAKLUMAT KLINIKAL
04.1 Petunjuk terapeutik
Rawatan akut sakit kepala migrain dengan atau tanpa aura.
04.2 Posologi dan kaedah pentadbiran
Dos tablet Zomig yang disyorkan untuk rawatan serangan migrain adalah 2.5 mg. Dianjurkan agar tablet Zomig diambil secepat mungkin setelah bermulanya sakit kepala migrain, namun ia berkesan walaupun diambil pada peringkat kemudian.
Tablet harus ditelan keseluruhan dan dengan air.
Sekiranya gejala migrain muncul semula dalam 24 jam dari tindak balas awal, dos kedua mungkin diambil. Sekiranya dos kedua diperlukan, ini tidak boleh diambil sehingga 2 jam setelah dos awal. Sekiranya pesakit tidak memberi tindak balas terhadap dos pertama. dos kedua tidak mungkin bermanfaat semasa serangan yang sama.
Sekiranya pesakit tidak mencapai tindak balas yang memuaskan dengan dos 2.5 mg, dos Zomig 5 mg boleh dipertimbangkan untuk serangan berikutnya.
Jumlah dos harian tidak boleh melebihi 10 mg. Zomig tidak boleh diambil lebih dari 2 dos dalam jangka masa 24 jam.
Zomig tidak ditunjukkan untuk profilaksis migrain.
Penggunaan pada kanak-kanak (di bawah 12 tahun)
Keselamatan dan keberkesanan tablet zolmitriptan pada pesakit pediatrik belum dinilai. Oleh itu, penggunaan Zomig pada kanak-kanak tidak digalakkan.
Remaja (12-17 tahun)
Keberkesanan tablet Zomig belum ditunjukkan dalam percubaan klinikal terkawal plasebo pada pesakit berusia 12-17 tahun. Oleh itu, penggunaan tablet Zomig pada remaja tidak digalakkan.
Gunakan pada pesakit yang berumur lebih dari 65 tahun
Keselamatan dan keberkesanan zolmitriptan pada pesakit yang berusia lebih dari 65 tahun belum ditentukan. Oleh itu, penggunaan Zomig pada orang tua tidak digalakkan.
Pesakit dengan kekurangan hepatik
Metabolisme zolmitriptan dikurangkan pada pasien dengan kekurangan hati (lihat bahagian 5.2). Bagi pesakit dengan kekurangan hati sederhana atau teruk, disyorkan dos maksimum 5 mg dalam 24 jam. Walau bagaimanapun, tidak diperlukan penyesuaian dos untuk pesakit dengan kekurangan. penyakit hati ringan.
Pesakit dengan kekurangan buah pinggang
Tidak diperlukan penyesuaian dos pada pesakit dengan pelepasan kreatinin melebihi 15 mL / min. (lihat bahagian 4.3 dan bahagian 5.2).
Interaksi yang memerlukan penyesuaian dos (lihat bahagian 4.5)
Dos maksimum 5 mg dalam 24 jam disyorkan pada pesakit yang menggunakan perencat MAO-A.
Dos maksimum 5 mg zolmitriptan dalam 24 jam disyorkan pada pesakit yang mengambil cimetidine.
Pada pesakit yang mengambil inhibitor khusus CYP 1A2, seperti fluvoxamine dan quinolones (mis. Ciprofloxacin), disyorkan dos maksimum 5 mg zolmitriptan dalam 24 jam.
04.3 Kontraindikasi
Zomig dikontraindikasikan pada pesakit dengan hipersensitiviti yang diketahui terhadap zolmitriptan atau mana-mana eksipien.
Hipertensi sederhana atau teruk dan hipertensi ringan yang tidak terkawal.
Kelas sebatian ini (agonis reseptor 5HT1B / 1D) telah dikaitkan dengan vasospasme koronari, akibatnya pesakit dengan penyakit jantung iskemik dikeluarkan dari ujian klinikal.
Oleh itu, Zomig tidak boleh digunakan pada pesakit yang mengalami infark miokard atau yang mempunyai penyakit jantung iskemia, vasospasme koroner (Prinzmetal's angina), penyakit vaskular periferal atau kepada pesakit yang mempunyai gejala atau tanda-tanda yang menunjukkan penyakit jantung iskemia.
Pemberian zolmitriptan bersamaan dengan ergotamin, derivatif ergotamin (termasuk metysergide), sumatriptan, naratriptan dan agonis reseptor 5HT1B / 1D yang lain adalah kontraindikasi (lihat bahagian 4.5).
Zolmitriptan tidak boleh diberikan kepada pesakit dengan riwayat kemalangan serebrovaskular (ACV) atau serangan iskemia sementara (TIA).
Zolmitriptan dikontraindikasikan pada pesakit dengan pelepasan kreatinin di bawah 15 ml / min.
04.4 Amaran khas dan langkah berjaga-jaga yang sesuai untuk digunakan
Zolmitriptan hanya boleh diberikan apabila diagnosis migrain jelas dibuat. Seperti terapi akut lain untuk migrain, perlu berhati-hati untuk mengesampingkan keadaan neurologi berpotensi serius yang lain sebelum merawat sakit kepala pada pesakit yang sebelumnya tidak didiagnosis sebagai migrain dan pada pesakit migrain yang mengalami gejala atipikal. Digunakan pada migrain hemiplegik, basilar atau oftalmoplegik. kejadian serebrovaskular telah dijelaskan pada pesakit yang dirawat dengan agonis reseptor 5HT1B / 1D. Harus diingat bahawa penghidap migrain mungkin berisiko untuk beberapa kejadian serebrovaskular.
Zolmitriptan tidak boleh diberikan kepada pesakit dengan sindrom Wolff-Parkinson-White simptomatik atau aritmia yang berkaitan dengan laluan aksesori konduksi jantung yang lain.
Vasospasme koronari, angina pectoris dan infark miokard telah dilaporkan dalam kes yang sangat jarang berlaku, seperti pada agonis reseptor 5HT1B / 1D yang lain.
Zomig tidak boleh diberikan kepada pesakit dengan faktor risiko penyakit jantung iskemia (seperti merokok, hipertensi, hiperlipidemia, diabetes mellitus, keturunan) tanpa melakukan penilaian kardiovaskular terlebih dahulu (lihat bahagian 4.3).Perhatian khusus harus diberikan kepada wanita dan lelaki pascamenopause yang berumur lebih dari 40 tahun dengan faktor risiko ini.
Namun, melalui penilaian seperti itu, tidak selalu mungkin untuk mengenal pasti semua pesakit dengan penyakit jantung, dan dalam kes yang sangat jarang berlaku, pesakit tanpa penyakit kardiovaskular yang mendasari telah mengalami kejadian jantung yang serius.
Seperti agonis reseptor 5HT1B / 1D yang lain, berat, sesak atau ketegangan prekordial telah dijelaskan berikutan pemberian zolmitriptan (lihat bahagian 4.8).
Sekiranya sakit dada atau gejala yang menunjukkan penyakit jantung iskemik muncul, tidak perlu diambil dos zolmitriptan lagi sehingga penilaian perubatan yang tepat telah dibuat.
Seperti agonis reseptor 5HT1B / 1D yang lain, peningkatan sementara dalam tekanan darah sistemik telah dilaporkan pada pesakit dengan atau tanpa riwayat hipertensi. Jarang sekali, peningkatan tekanan darah ini dikaitkan dengan kejadian klinikal yang ketara.
Dos zolmitriptan yang disyorkan tidak boleh melebihi.
Kesan sampingan mungkin lebih biasa semasa penggunaan triptan dan sediaan herba yang mengandungi St. John's wort (Hypericum perforatum).
Sindrom Serotonin (termasuk perubahan status mental, ketidakstabilan autonomi dan kelainan neuromuskular) telah dilaporkan berikutan rawatan bersamaan dengan triptan dan perencat pengambilan serotonin selektif (SSRI) atau perencat pengambilan serotonin dan norepinefrin (SNRI). Reaksi ini boleh menjadi teruk. Sekiranya rawatan bersamaan dengan zolmitriptan dan SSRI atau SNRI dibenarkan secara klinis, disarankan agar pesakit dijaga di bawah pengamatan yang memadai, terutama pada awal perawatan, jika terjadi peningkatan dos atau penambahan ubat serotonergik lain (lihat paragraf 4.5) .
Penggunaan ubat penghilang rasa sakit yang berpanjangan untuk rawatan sakit kepala dapat memperburuk keadaan. Sekiranya keadaan ini berlaku atau disyaki, doktor harus berunding dan rawatan dihentikan. Diagnosis sakit kepala penyalahgunaan ubat harus disyaki pada pesakit yang mengalami sakit kepala yang kerap atau setiap hari walaupun ( atau kerana) penggunaan ubat sakit kepala secara berkala.
Produk ubat ini mengandungi laktosa. Pesakit dengan masalah keturunan yang jarang berlaku terhadap intoleransi galaktosa, kekurangan Lapp laktase atau penyerapan glukosa-galaktosa tidak boleh mengambil ubat ini.
04.5 Interaksi dengan produk ubat lain dan bentuk interaksi lain
Kajian interaksi telah dilakukan dengan kafein, ergotamin, dihydroergotamine, paracetamol, metoclopramide, pizotifen, fluoxetine, rifampicin dan propranolol tanpa perbezaan yang relevan secara klinikal dalam farmakokinetik zolmitriptan atau metabolit aktifnya yang diperhatikan.
Data dari subjek sihat menunjukkan bahawa tidak ada interaksi farmakokinetik atau klinikal yang signifikan antara zolmitriptan dan ergotamine. Walau bagaimanapun, peningkatan risiko vasospasme koronari adalah kemungkinan teoritis dan pemberian bersamaan adalah kontraindikasi. Sebaiknya tunggu sekurang-kurangnya 24 jam setelah penggunaan sediaan yang mengandung ergotamin sebelum memberikan zolmitriptan. Sebaliknya, disarankan untuk menunggu sekurang-kurangnya enam jam setelah pemberian zolmitriptan sebelum memberikan produk yang mengandung ergotamin (lihat bahagian 4.3).
Selepas pemberian moclobemide, perencat MAO-A tertentu, terdapat sedikit peningkatan (26%) dalam AUC zolmitriptan dan peningkatan AUC metabolit aktif 3 kali ganda. Oleh itu, pada pesakit yang dirawat dengan perencat MAO-A, pengambilan maksimum zolmitriptan 5 mg dalam 24 jam adalah disyorkan.
Selepas pemberian cimetidine, perencat umum sitokrom P450, waktu hayat dan AUC zolmitriptan masing-masing meningkat sebanyak 44% dan 48%. Tambahan pula, separuh hayat dan AUC metabolit N-desmethyl aktif (183C91) meningkat dua kali ganda.
Oleh itu, pada pesakit yang mengambil cimetidine, disyorkan dos zolmitriptan 24 jam tidak melebihi 5 mg.
Berdasarkan profil interaksi umum, interaksi dengan perencat tertentu CYP 1A2 tidak dapat dikecualikan. Oleh itu, dengan bahan jenis ini, seperti fluvoxamine dan quinolones (contohnya ciprofloxacin), disyorkan pengurangan dos yang sama.
Selegiline (perencat MAO-B) dan fluoxetine (SSRI) tidak menyebabkan interaksi farmakokinetik dengan zolmitriptan. Walau bagaimanapun, terdapat laporan pesakit dengan gejala yang sesuai dengan sindrom serotonin (termasuk perubahan status mental, ketidakstabilan autonomi, dan kelainan neuromuskular) berikutan penggunaan perencat pengambilan serotonin selektif (SSRI) atau perencat pengambilan serotonin dan serotonin. triptans (lihat bahagian 4.4).
Seperti agonis 5HT1B / 1D lain, zolmitriptan boleh melambatkan penyerapan produk ubat lain.
Pemberian bersamaan dengan agonis 5HT1B / 1D lain dalam masa 24 jam selepas rawatan dengan zolmitriptan harus dielakkan. Begitu juga dengan pemberian zolmitriptan dalam masa 24 jam setelah menggunakan agonis 5HT1B / 1D yang lain.
04.6 Kehamilan dan penyusuan
Kehamilan
Keselamatan produk ubat ini untuk digunakan dalam kehamilan belum terbukti pada wanita. Penilaian kajian eksperimental pada haiwan tidak menunjukkan kesan teratogenik langsung. Walau bagaimanapun, beberapa hasil kajian embriooksisiti menunjukkan penurunan daya maju embrio. Zolmitriptan hanya perlu dipertimbangkan jika faedah yang diharapkan kepada ibu adalah lebih besar daripada risiko yang mungkin timbul pada janin.
Masa makan
Kajian pada haiwan menyusui menunjukkan bahawa zolmitriptan masuk ke dalam susu. Tidak ada data mengenai perjalanan zolmitriptan ke dalam susu ibu. Oleh itu, berhati-hati harus dilakukan semasa berhasrat untuk memberikan zolmitriptan kepada wanita yang menyusui. Pendedahan bayi harus dikurangkan dengan mengelakkan penyusuan selama 24 jam selepas rawatan.
04.7 Kesan terhadap kemampuan memandu dan menggunakan mesin
Dalam sekumpulan kecil individu yang sihat tidak ada bukti penurunan prestasi psikomotor yang signifikan, dinilai dengan ujian, dengan dosis hingga 20 mg zolmitriptan. Perhatian disarankan pada pasien yang melakukan tugas yang memerlukan perhatian (misalnya memandu atau mengoperasikan mesin) kerana rasa mengantuk dan gejala lain mungkin terjadi semasa serangan migrain.
04.8 Kesan yang tidak diingini
Kesan sampingan yang mungkin berlaku secara sementara, cenderung berlaku dalam masa empat jam selepas pentadbiran, penggunaan berulang tidak meningkatkan kekerapan dan hilang secara spontan tanpa rawatan lanjut.
Definisi berikut merujuk kepada kejadian kesan yang tidak diingini:
Sangat biasa (≥1 / 10); biasa (≥1 / 100,
Dalam setiap kumpulan frekuensi, kesan yang tidak diingini ditunjukkan dalam tahap keseriusan.
Kesan yang tidak diingini berikut telah dilaporkan berikutan pemberian zolmitriptan:
Beberapa gejala mungkin merupakan bahagian dari serangan migrain itu sendiri.
Melaporkan tindak balas buruk yang disyaki
Melaporkan tindak balas buruk yang disyaki berlaku selepas kebenaran produk ubat adalah penting kerana ia memungkinkan pemantauan berterusan terhadap keseimbangan manfaat / risiko produk ubat tersebut. Profesional penjagaan kesihatan diminta untuk melaporkan sebarang reaksi buruk yang disyaki melalui sistem pelaporan nasional. "Alamat www. agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosis
Pemberian 50 mg, dalam satu dos oral, kepada sukarelawan sering mengakibatkan bermulanya penenang.
Waktu paruh penghapusan tablet zolmitriptan adalah 2.5 hingga 3 jam (lihat bahagian 5.2) dan oleh itu, sekiranya berlaku overdosis dengan tablet Zomig, pemantauan pesakit harus berterusan sekurang-kurangnya 15 jam atau selagi tanda atau gejala berterusan.
Tidak ada penawar khusus untuk zolmitriptan. Sekiranya mabuk teruk, prosedur perawatan intensif dianjurkan, termasuk pembentukan dan pemeliharaan saluran udara paten, sokongan oksigenasi dan pengudaraan yang mencukupi, pemantauan dan sokongan fungsi kardiovaskular.
Kesan hemodialisis dan dialisis peritoneal pada kepekatan zolmitriptan serum tidak diketahui.
05.0 HARTA FARMAKOLOGI
05.1 Sifat farmakodinamik
Kumpulan farmakoterapi: agonis serotonin selektif (reseptor 5HT1)
Kod ATC: N02CC03.
Zolmitriptan telah terbukti menjadi agonis selektif reseptor 5HT1B / 1D yang menjadi pengantara kontraksi vaskular.Zolmitriptan mempunyai pertalian tinggi untuk reseptor rekombinan manusia, 5HT1B dan 5HT1D dan pertalian sederhana untuk reseptor 5HT1A. Zolmitriptan tidak mempunyai pertalian yang signifikan atau aktiviti farmakologi terhadap subtipe reseptor 5HT yang lain (5HT2, 5HT3, 5HT4) atau terhadap reseptor adrenergik, histamin, muscarinic atau dopaminergik.
Pada model haiwan, pemberian zolmitriptan menyebabkan vasokonstriksi pada peredaran arteri karotid. Selanjutnya, kajian eksperimental yang dilakukan pada haiwan menunjukkan bahawa zolmitriptan menghalang aktiviti saraf trigeminal secara pusat dan perifer, dengan penghambatan pelepasan neuropeptida (peptida berkaitan gen calcitonin (CGRP), peptida usus vasoaktif (VIP) dan Bahan P).
Dalam ujian klinikal, permulaan keberkesanan berlaku setelah satu jam, dengan peningkatan keberkesanan pada sakit kepala dan gejala migrain lain, seperti mual, fotofobia dan fonofobia, yang diperhatikan antara 2 dan 4 jam.
Zolmitriptan berkesan secara konsisten dalam migrain dengan atau tanpa aura dan migrain yang berkaitan dengan kitaran haid. Zolmitriptan, ketika diambil semasa aura, belum terbukti dapat mencegah sakit kepala migrain dan oleh itu Zomig harus diambil semasa fasa sakit kepala migrain.
Pada 696 remaja dengan migrain, pada dos 2.5 mg, 5 mg dan 10 mg, kajian klinikal terkawal gagal menunjukkan kelebihan tablet zolmitriptan berbanding plasebo. Keberkesanannya belum terbukti.
05.2 Sifat farmakokinetik
Pada manusia, zolmitriptan diserap dengan cepat dan baik (sekurang-kurangnya 64%) selepas pemberian oral. Rata-rata bioavailabiliti sebatian induk adalah sekitar 40%. Terdapat metabolit aktif (metabolit N-desmethyl), juga "dengan 5HT1B / Aktiviti agonis 1D, yang 2 hingga 6 kali lebih kuat daripada zolmitriptan pada model haiwan.
Pada subjek yang sihat, selepas pemberian satu dos, zolmitriptan dan metabolit aktifnya, metabolit N-desmethyl, menunjukkan AUC dan C berkadar dosis melebihi julat dos 2.5 hingga 50 mg. Penyerapan zolmitriptan cepat. Pada subjek sukarelawan yang sihat, 75% Cmax dicapai dalam 1 jam, setelah itu kepekatan zolmitriptan plasma dipertahankan pada tahap ini sehingga 4-5 jam setelah dos.
Penyerapan zolmitriptan tidak dipengaruhi oleh kehadiran makanan. Tidak ada bukti pengumpulan setelah penggunaan zolmitriptan berulang.
Kepekatan plasma zolmitriptan dan metabolitnya lebih rendah dalam 4 jam pertama selepas pemberian ubat semasa migrain daripada pada masa bebas migrain, menunjukkan kelewatan penyerapan sesuai dengan penurunan kadar pengosongan gastrik. Dilihat semasa serangan migrain.
Zolmitriptan dihilangkan secara meluas oleh metabolisme hepatik diikuti oleh perkumuhan metabolit urin. Terdapat tiga metabolit utama: asid asetik indole (metabolit utama dalam plasma dan air kencing) dan analog N-teroksidasi dan N-demetilasi. Metabolit N-desmethyl aktif, sementara dua yang lain tanpa aktiviti. Kepekatan plasma metabolit N-desmethyl adalah lebih kurang separuh daripada produk induk, dan oleh itu diharapkan dapat menyumbang kepada kesan terapi Zomig. Lebih daripada 60% dos oral tunggal dikeluarkan dalam air kencing (terutamanya dalam bentuk metabolit asid asetik indole) dan kira-kira 30% dikeluarkan dalam najis, terutamanya sebagai produk yang tidak berubah.
Selepas pemberian intravena, rata-rata pelepasan plasma kira-kira 10 mL / min / kg, di mana satu perempat adalah pelepasan ginjal. Pelepasan ginjal lebih tinggi daripada kadar penapisan glomerular, menunjukkan adanya rembesan tiub ginjal. Isipadu pengedaran selepas pemberian intravena ialah 2.4 L / kg.Pengikatan zolmitriptan dan metabolit N-desmethyl ke protein plasma rendah (kira-kira 25%). Waktu paruh penghapusan zolmitriptan adalah 2.5 hingga 3. Jam paruh metabolitnya serupa, menunjukkan bahawa penghapusannya adalah proses yang dibatasi oleh kadar pembentukan.
Pelepasan zolmitriptan dan semua metabolitnya dikurangkan (7-8 kali ganda) pada pesakit dengan gangguan buah pinggang sederhana atau teruk berbanding dengan subjek yang sihat, walaupun AUC sebatian induk dan metabolit aktifnya hanya sedikit lebih tinggi. (Masing-masing 16% dan 35 %), dengan kenaikan satu "jam, atau hingga 3 dan 3.5 jam, pada waktu paruh. Parameter ini berada dalam jangkauan yang dilihat pada sukarelawan yang sihat.
Satu kajian yang dilakukan untuk menilai kesan gangguan hati terhadap farmakokinetik zolmitriptan menunjukkan bahawa AUC dan Cmax masing-masing meningkat sebanyak 94% dan 50% pada pesakit dengan gangguan hati sederhana dan masing-masing sebanyak 226% dan 47%. Dengan kekurangan hati yang teruk berbanding dengan sukarelawan yang sihat. Pendedahan terhadap metabolit, termasuk metabolit aktif, berkurang.Untuk metabolit aktif 183C91, AUC dan Cmax masing-masing dikurangkan sebanyak 33% dan 44% pada pesakit dengan gangguan hati sederhana dan 82% dan 90% pada pesakit dengan kekurangan hati yang teruk.
Profil farmakokinetik zolmitriptan pada subjek tua yang sihat adalah serupa dengan yang dilihat pada sukarelawan muda yang sihat.
05.3 Data keselamatan praklinikal
Kesan praklinikal dalam kajian ketoksikan dos tunggal dan berulang diperhatikan hanya pada pendedahan yang jauh melebihi pendedahan maksimum manusia.
Berdasarkan hasil kajian ketoksikan genetik in vivo dan in vitro, kesan genotoksik zolmitriptan tidak dijangkakan dalam keadaan penggunaan klinikal yang normal.
Tidak ada tumor yang berkaitan secara klinikal yang diperhatikan dalam kajian karsinogenisiti pada tikus dan tikus.
Seperti agonis reseptor 5HT1B / 1D lain, zolmitriptan mengikat melanin.
06.0 MAKLUMAT FARMASI
06.1 Eksipien
Laktosa anhidrat
Selulosa mikrokristalin
Natrium pati glikolat (jenis A)
Magnesium stearat
Hypromellose
Macrogol (400 dan 8000)
Besi oksida (E 172: tablet kuning - 2.5 mg; merah - tablet 5 mg)
Titanium dioksida (E 171).
06.2 Ketidaksesuaian
Tidak relevan.
06.3 Tempoh sah
3 tahun.
06.4 Langkah berjaga-jaga khas untuk penyimpanan
Jangan simpan di atas 30 ° C.
06.5 Sifat pembungkusan segera dan kandungan bungkusan
Tablet 2.5 atau 5 mg yang dibungkus dalam lepuh yang mengandungi: 3, 6 (dengan atau tanpa bekas), 12 atau 18 tablet.
Lepuh diperbuat daripada poliamida Al-PVC / Al.
Tidak semua saiz pek boleh dipasarkan.
06.6 Arahan penggunaan dan pengendalian
Tiada arahan khas.
07.0 PEMEGANG KEBENARAN PEMASARAN
AstraZeneca S.p.A.
Istana Volta
Melalui F. Sforza
Basiglio (MI)
08.0 NOMBOR KEBENARAN PEMASARAN
"Tablet bersalut filem 2.5 mg" 3 tablet dalam al-pvc / al A.I.C. 033345012
"Tablet bersalut filem 2.5 mg" 6 tablet dalam al-pvc / al A.I.C. 033345024
"Tablet bersalut filem 2.5 mg" 6 tablet dalam lepuh al-pvc / al dengan A.I.C. 033345036
"Tablet bersalut filem 2.5 mg" 12 tablet dalam al-pvc / al A.I.C. 033345048
"Tablet bersalut filem 2.5 mg" 18 tablet dalam al-pvc / al A.I.C. 033345051
"Tablet bersalut filem 5 mg" 3 tablet dalam al-pvc / al A.I.C. 033345063
"Tablet bersalut filem 5 mg" 6 tablet dalam al-pvc / al A.I.C. 033345075
"Tablet bersalut filem 5 mg" 6 tablet dalam lepuh al-pvc / al dengan A.I.C. 033345087
"Tablet bersalut filem 5 mg" 12 tablet dalam al-pvc / al A.I.C. 033345099
"Tablet bersalut filem 5 mg" 18 tablet dalam al-pvc / al A.I.C. 033345101
09.0 TARIKH KEBENARAN ATAU PEMBAHARUAN KEBENARAN
Tarikh kebenaran pertama: 7 Ogos 1997
Tarikh pembaharuan terakhir: 30 November 2006.
10.0 TARIKH SEMAKAN TEKS
Jun 2015